C(sp3)–C(sp3)鍵構成了許多生物活性天然產物、藥物和功能材料的骨架。研究表明,sp3雜化手性碳的較高豐度與藥物發現中改進的效力、選擇性和可專利性密切相關。因此,開發能夠同時形成C(sp3)–C(sp3)鍵并控制立體化學的高效方法一直是合成化學中長期關注的課題。然而,實現相鄰完全取代碳立體中心的非對映和對映選擇性構建仍然是一個艱巨的挑戰,這主要是由于空間位阻增加導致的不利熱力學和動力學效應。
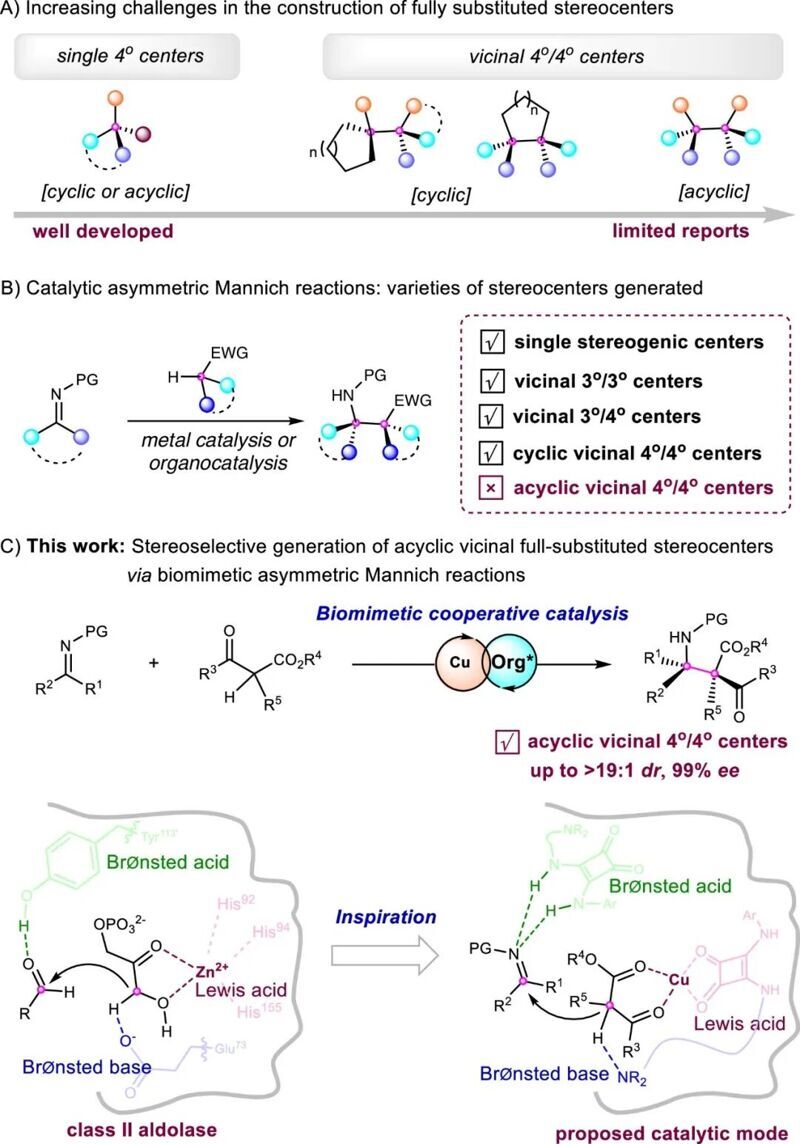
圖1 構建完全取代立體中心的挑戰以及導致生成無環相鄰四取代立體中心的仿生不對稱曼尼希反應的發展
中山大學翁江、魯桂聯合南方科技大學余沛源等研究者報告了一種仿生銅/方酰胺協同催化策略,用于挑戰性的無環酮亞胺和α-取代β-酮酯之間的不對稱曼尼希反應。獲得了具有相鄰無環四取代立體中心的高度功能化曼尼希加合物,并表現出良好的產率和優異的立體選擇性(高達>19:1 dr和99% ee)。這些對映體純產物的多功能性通過其具有完全非對映控制的多樣化轉化得到進一步凸顯。機理研究和DFT計算支持了銅和方酰胺在底物活化和立體選擇性控制中的新型協同作用。
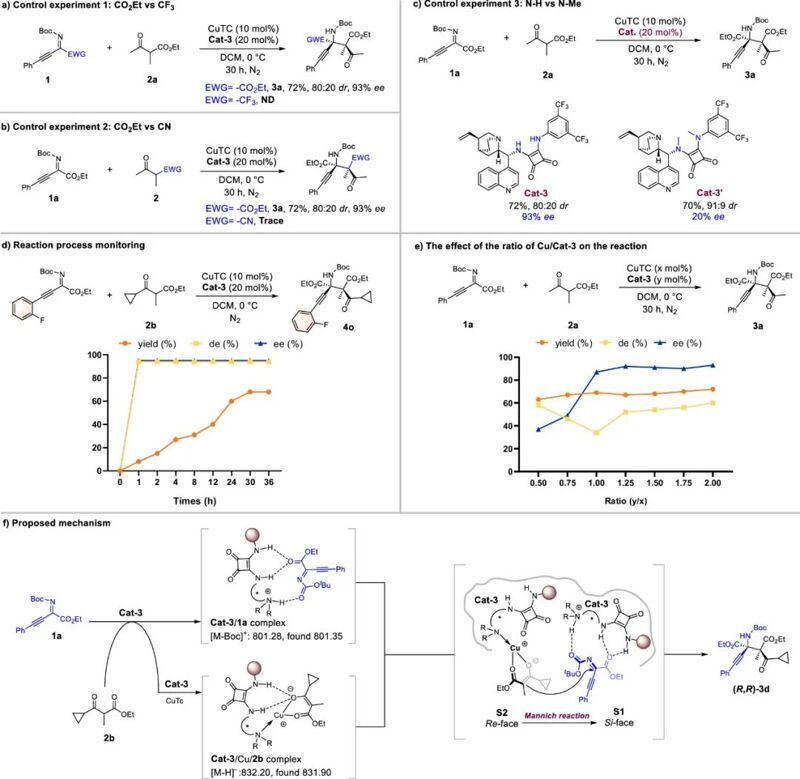
圖2 對照實驗和機理研究
總之,受II類醛縮酶的啟發,該項研究開發了一種仿生銅-方酰胺協同催化策略用于不對稱曼尼希反應,實現了在無環系統中便捷地構建相鄰四取代立體中心。利用無環酮亞胺和空間位阻的α-取代β-酮酯作為挑戰性曼尼希底物,成功合成了具有相鄰無環四取代立體中心的高度功能化氨基酸衍生物,并具有優異的非對映和對映選擇性(高達>19:1 dr和99% ee)。初步機理研究和DFT計算表明,該策略的成功歸因于銅鹽和叔胺-方酰胺有機催化劑的協同作用,這些作用對于底物活化和立體選擇性控制至關重要。
Zhu, WR., Ouyang, ZL., Du, X. et al. Accessing acyclic vicinal tetrasubstituted stereocenters via biomimetic Cu/squaramide cooperative catalysed asymmetric Mannich reactions. Nat Commun 16 8896 (2025). https://doi.org/10.1038/s41467-025-63919-9








