介紹一篇發表在Nature上的文章“Hijacking a bacterial ABC transporter for genetic code expansion”,通訊作者是來自蘇黎世聯邦理工學院的Kathrin Lang教授,她的主要研究方向是遺傳密碼擴展和體內新型化學反應。

在遺傳密碼擴展技術(Genetic Code Expansion, GCE)中,非天然氨基酸(ncAA)的細胞攝取效率低是限制蛋白質合成效率的一大因素。針對這一問題,本文作者創新性地提出了一種“劫持”細菌轉運系統(尤其是寡肽轉運系統Opp)的新策略,通過將異肽鍵連接的三肽(Z-XisoK)作為“特洛伊木馬”,將其轉運進入細菌中后三肽切割即可釋放ncAA,最終實現ncAA的高效導入與編碼的目的。

在實驗中,作者設計并合成了一系列異肽鍵連接的三肽(如G-AisoK、G-SisoK等),其中XisoK為待導入的ncAA。這些三肽可通過固相肽合成方便獲得。通過構建大腸桿菌轉運系統(如OppA、OppB、OppC、OppD等)各個蛋白的敲除株,作者證實了Opp轉運系統在三肽攝取中的核心作用。異肽鍵三肽可被Opp系統主動攝取,并在胞內被肽酶切割釋放ncAA,顯著提高了胞內ncAA濃度(比直接添加高5–10倍),從而顯著提升ncAA的編碼效率。OppA(周質結合蛋白)及其下游轉運組分(OppB/C/D)共同實現對三肽的轉運,其中OppA對三肽的識別主要依賴其N端和C端結構,而非側鏈,因而具有良好的底物兼容性。隨后,通過構建肽酶(如PepA、PepN)敲除株,結合蛋白表達分析,作者確定三肽在胞內被是被肽酶切割從而釋放ncAA。
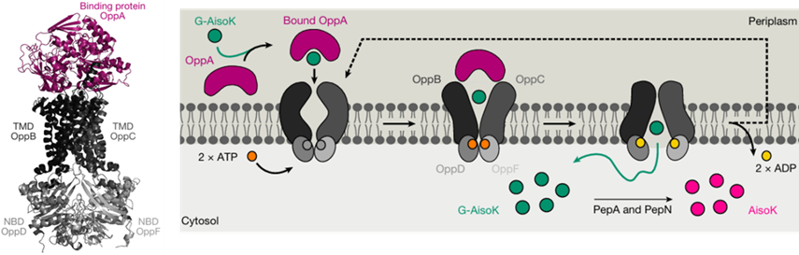
在實現方法構建和機制闡釋后,作者嘗試將該系統進一步擴展,以實現更廣泛的GCE應用。首先,作者建立通用G-XisoK工具箱,導入多種功能ncAA。隨后,為解決三肽在富營養培養基(如2-YT)中被競爭性抑制的問題,作者通過定向進化OppA實現富營養培養基中的高效表達。

最后,作者通過改變三肽N端殘基(Z),可導入原本難以進入細胞的ncAA(如帶負電或體積大的殘基),如光交聯劑、生物正交基團、PTM類似物等。作者合成14的種Z-AisoK三肽中,8種可在野生型中高效導入,6種需工程化的OppA變體。更重要的是,作者實現了雙重ncAA共導入:通過設計含有兩個不同ncAA的三肽(如AcK-pLisoK),利用正交的PylRS/tRNA系統,即可實現單個蛋白中兩個不同ncAA的共編碼,為研究翻譯后修飾與蛋白相互作用提供了新工具。

總的來說,本文開發了一種模塊化、可進化、通用性強的ncAA導入新策略,通過工程化細菌ABC轉運系統,使ncAA的導入不再依賴其自身膜通透性,而是通過三肽載體和可進化的OppA變體實現,極大拓展了GCE的化學空間和實用性,為蛋白質工程、合成生物學和生物藥物開發提供了強有力的工具平臺。
本文作者:FTY
責任編輯:MB
DOI:10.1038/s41586-025-09576-w
原文鏈接:https://doi.org/10.1038/s41586-025-09576-w








