文|二甲亞砜 編|來蘇兒 圖|來源于網絡
1
(1)底物結構對SN1反應的影響
決定SN1反應速度的是C+穩定性。越是穩定的C+,越容易生成。
∵C+穩定性:3°>2°>1°>CH3+
∴SN1反應活性:3°RX >2°RX >1°RX > CH3X
(2)底物結構對SN2反應的影響
決定SN2反應速度的是過渡態的穩定性。過渡態越穩定,反應的活化能越低,反應速度越快。
影響SN2過渡態穩定性的主要因素:
空間位阻:α-C上取代基越多,Nu-越不易接近α-C,過渡態也越不穩定
∴SN2反應活性:CH3X>1°RX>2°RX>3°RX
(3)幾種特殊鹵代烴烷基對親核取代反應活性的影響
(i)乙烯型鹵代烴
以氯乙烯為例:

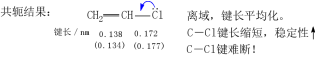
∴ 乙烯型鹵代烯烴的化學性質:
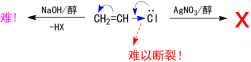
∴ 氯苯和氯乙烯在SN1和SN2反應都不活潑
(ii)烯丙型鹵代烴
烯丙型鹵代烯烴中的C-X鍵易斷! 例:
對于雙分子反應:
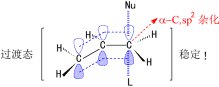
對于單分子反應:
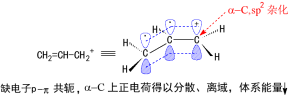
烯丙型鹵代烯烴的特殊活潑性是由于親核取代反應的中間體或過渡態穩定。
烯丙型(芐基型)鹵代烴的結構與反應特征:
①鹵原子活性非常高,容易發生取代反應
②烯丙型鹵代烴SN1反應時有重排
③消除反應生成穩定的共軛二烯烴
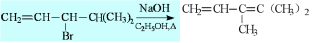
綜上所述:
→1°RX主要進行SN2反應;
→2°RX同時進行SN1和SN2,但SN1和SN2速度都很慢。
→3°RX主要進行SN1反應;
2
試劑的親核性對SN1反應速率基本沒影響;試劑的親核性↑,有利于SN2。
親核性——試劑親碳原子核的能力
(1)反應速率比較:
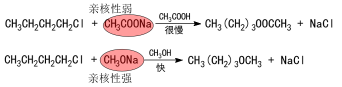
(2)試劑的親核性的決定因素
主要由兩個因素決定:堿性和可極化性。這兩個因素對試劑的親核性的影響有時是一致的,有時不一致。
一致:同一原子或同一周期的原子作為親核中心時,試劑的親核性與堿性有相同的強弱次序。
例1:親核性:C2H5O->HO->CH3COO->C2H5OH>H2O
例2:親核性:NH2->HO->F-, NH3>H2O
不一致:同一族的原子作為親核中心時,變形性大者呈現出較強的親核性。從上到下,體積依次增大,親核性依次增強這與堿性的強弱次序相反。
堿性: F->Cl- > Br- >I-
親核性:F- < Cl- < Br- < I
原因:F-離子半徑小,電荷集中,原子核對核外電子的束縛力強,不容易極化,很難與碳原子結合。
I-離子半徑大,原子核對核外電子的束縛力較差,容易極化,易與碳原子結合。
3 溶劑極性的影響
極性強的質子溶劑有利于SN1,極性弱的非質子性溶劑對SN2反應有利。
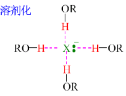
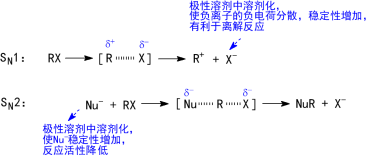
4 離去基團(鹵原子)的影響
SN2和SN1反應的慢步驟都包括C-X的斷裂,因此離去基團X-的性質對SN2和SN1反應將產生相似的影響:
SN1和SN2反應活性:R-I>R-Br>R-Cl>R-F
原因:C-X鍵弱,X-容易離去,C-X鍵強,X-不容易離去。
C-X鍵的強弱主要與X的電負性有關。
總結: 影響親核取代反應歷程的因素
(1)底物結構:
1°RX主要進行SN2反應;
2°RX同時進行SN1和SN2,但SN1和SN2速度都很慢。
3°RX主要進行SN1反應
(2)親核試劑:
試劑的親核性對SN1反應速率基本沒影響;
試劑的親核性↑,有利于SN2。
(3)溶劑極性:
極性強的質子溶劑有利于SN1,極性弱的非質子性溶劑對SN2反應有利。
(4)離去基團:
SN2和SN1反應的慢步驟都包括C-X的斷裂,因此離去基團X-的性質對SN2和SN1反應將產生相似的影響。








