分享一篇發表在Nat. Chem. Biol.上的文章,題目為“Lipoyl deglutarylation by ABHD11 regulates mitochondrial and T cell metabolism”,通訊作者是劍橋大學的James A. Nathan與瑞典卡羅林斯卡研究所的Randall S Johnson,他們的研究方向包括細胞代謝與微環境調控。

戊二酸是賴氨酸和色氨酸分解代謝過程的產物之一,可以在細胞內進一步轉化為戊二酰輔酶A,也可游離存在。此前的研究表明,戊二酸能夠在蛋白質上形成翻譯后修飾,例如在Lys上形成的戊二酰化修飾,以及在硫辛酰化修飾上形成的戊二酰-硫辛酰加合物(Lpglu)。硫辛酰化修飾對于線粒體內一系列酶復合物(如OGDHc、PDHc等)的功能是至關重要的,作者在此前的研究中發現,戊二酸能夠與PDHc的硫辛酰化催化臂形成加合物,進而抑制其催化活性。此外,他們也發現絲氨酸水解酶ABHD11能夠維持OGDHc的戊二酰化修飾水平。綜合上述兩篇工作,作者猜想可能OGDHc上可能也會形成類似的戊二酰-硫辛酰加合物,且ABHD11可能在其中起到了去除加合物、恢復OGDHc催化活性的功能。
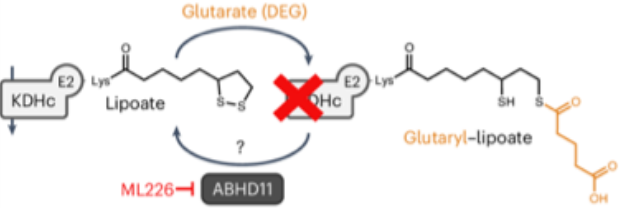
首先,作者在HeLa細胞系中證明,添加ABHD11的抑制劑ML226,或敲除ABHD11,都可以使OGDHc-E2亞基的硫辛酰化修飾水平降低,同時伴隨著Lpglu加合物的積累。LC-MS/MS結果也顯示,K110活性位點的Lpglu加合物水平在ABHD11敲除后發生了顯著的下降。接下來,作者將ABHD11純化,以OGDHc-E2中Lpglu位點的肽段作為底物,確定了ABHD11具有直接將Lpglu加合物水解的硫酯酶活性。
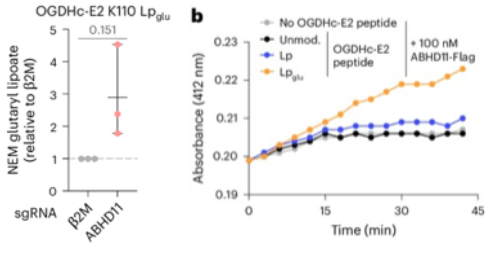
在功能層面,作者比較了ABHD11缺失與戊二酸(DEG)過載對細胞代謝的不同影響。先前的研究表明,ABHD11的缺失會導致2-OG積累,進而導致S-2-HG的形成,進一步導致一系列2-OG依賴性雙加氧酶(2-OGDDs)的失活。作者對這些生物過程的分析表明,ABHD11敲除能夠影響下游的一系列代謝通路,包括2-HG的積累、HIF-1α表達上調等,而DEG過載僅能夠增加游離戊二酸的水平。這些結果表明,ABHD11缺失是導致2-OG和2-HG積累和HIF-1激活的主要原因,而非戊二酸過載。
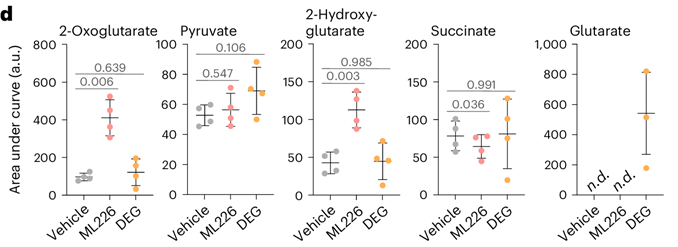
之后,作者也希望研究ABHD11對于T細胞功能的影響。此前的研究表明,激活的CD8+ T細胞中ABHD11表達水平會發生較為明顯的上調。因此,作者從健康人的外周血中分離出CD8+ T細胞,發現使用ML226抑制ABHD11的活性同樣可以抑制OGDHc的活性,但并未出現2-HG的積累,2-OGDD的活性也未被抑制。進一步的轉錄組和脂質組學分析發現,ABHD11抑制主要影響了脂肪酸代謝通路。脂肪酸合成和氧化過程對于記憶T細胞的維持十分重要,接下來的研究表明,ABHD11活性抑制導致的細胞內代謝重編程,會最終促進CCR7highCD45ROhigh的中央記憶表型(TCM)擴增,而減少CCR7lowCD45ROhigh的效應記憶表型(TEM)。此外,在模擬腫瘤微環境的低氧條件下,ML226處理的CD8+ T細胞分泌IFN-γ、Granzyme B和FasL的能力顯著下降,提示ABHD11的活性對于維持CD8+ T細胞在低氧條件下的效應功能至關重要。
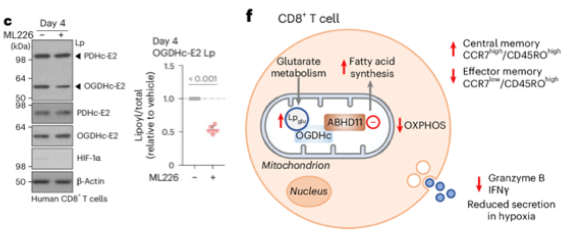
總之,本文揭示了ABHD11是一種特異性的戊二酰-硫辛酰化的硫酯酶,通過動態去除Lpglu修飾維持OGDHc功能與TCA循環穩態。
本文作者:YAQ
責任編輯:LYC
DOI:10.1038/s41589-025-01965-6
原文鏈接:https://doi.org/10.1038/s41589-025-01965-6








