介紹一篇發表在Nature chemical biology上的文章,題目為Cell-selective multiplexed bioorthogonal noncanonical amino acid tagging for nascent proteomics。通訊作者是來自波士頓學院的Eranthie Weerapana和Abhishek Chatterjee,他們課題組的研究方向分別是化學蛋白質組學和非經典氨基酸插入技術。

細胞蛋白質組是高度動態變化的,會響應內部和外部刺激而不斷變化,因此需要發展高靈敏且正交的策略來進行時間分辨的蛋白質組學解析,傳統細胞選擇性的生物正交ncAA標記(BONCAT)主要依賴于工程化的甲硫氨酰tRNA合成酶突變體MetRS-NLL,盡管其應用廣泛,卻存在明顯局限:標記速率有限,時間分辨率不足,缺乏多路復用能力。為解決這些問題,研究團隊將目光轉向了工程化的酪氨酰tRNA合成酶和色氨酰tRNA合成酶,它們能在極低表達水平下高效地將多種含點擊化學基團的非經典氨基酸摻入新合成蛋白質中。
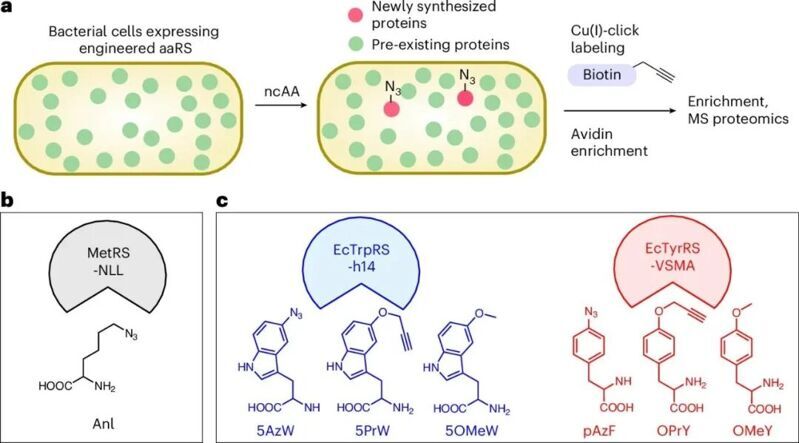
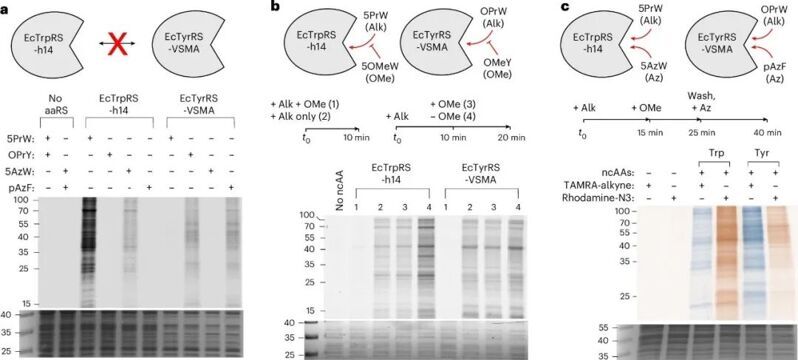
作者選擇了他們此前報道的兩種氨酰tRNA合成酶EcTrpRS-h14和EcTyrRS-VSMA,他們可以在加入帶有生物正交手柄的非經典氨基酸后僅一分鐘即可檢測到明顯的蛋白質標記信號,顯示出這兩種合成酶產生氨酰tRNA的高效性。兩種合成酶都可以識別對應氨基酸帶有不同生物正交基團的ncAA,而不會識別另一種氨基酸,表現出其進行多通道BONCAT蛋白質組學的潛力。
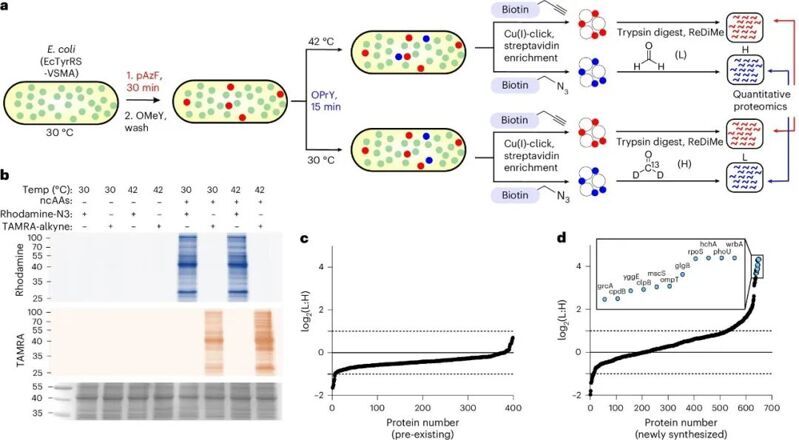
作者將這一策略應用在熱休克條件下新生蛋白質組學的鑒定中,他們先在使用正常溫度條件下用含炔基的底物標記預先存在的蛋白質組,然后在熱休克條件下用含疊氮的底物標記新合成的蛋白質,最后富集這兩組蛋白質進行質譜分析。結果顯示,熱休克主要影響新合成蛋白質組,包括多種分子伴侶和應激反應蛋白的表達上調,而預先存在的蛋白質組保持相對穩定。從而可以在單次實驗中同時捕捉新舊蛋白質組變化的能力。
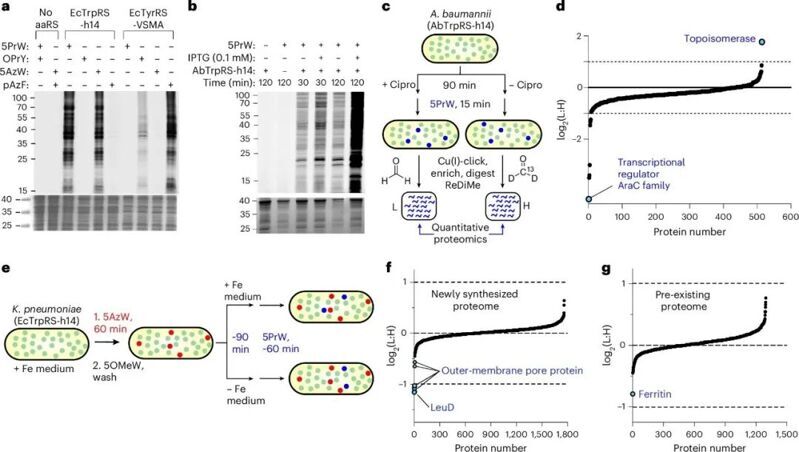
這一方法另一用是研究病原菌對于外界刺激的耐藥響應。對于同源性較低的鮑曼不動菌,團隊通過將關鍵活性位點突變“移植”至宿主自身的合成酶中,構建了適配宿主系統的工程酶,顯著提升了標記效率。在應用層面,他們利用該系統研究了環丙沙星處理對鮑曼不動桿菌蛋白質組的影響,發現細菌能感知并上調其靶標拓撲異構酶的表達,這可能是抗生素耐藥性產生的一種新機制。
總而言之,本文作者通過引入工程酪酰基-tRNA合成酶和色氨酸酰基-tRNA合成酶完成了新合成蛋白質的時間分辨表征。
本文作者:LYC
責任編輯:MB
DOI:10.1038/s41589-025-02039-3
原文鏈接:https://doi.org/10.1038/s41589-025-02039-3








