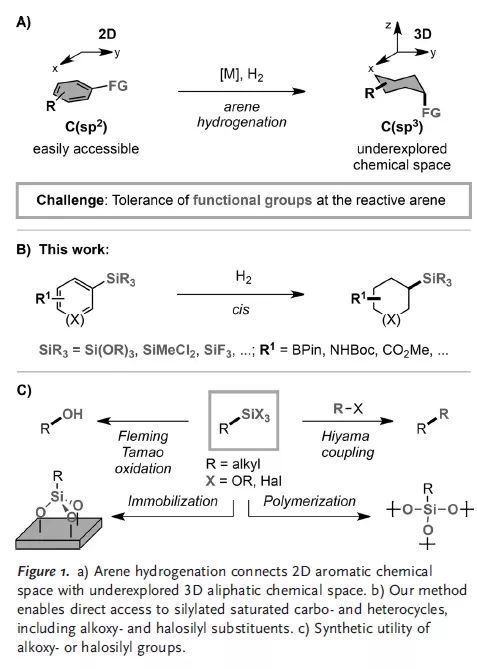
芳烴氫化可將具有二維平面結構的芳環直接轉化為具有三維空間的環己烷化合物,因此在藥物化學等領域具有重要的戰略價值。然而,芳環上的某些官能團可能會抑制該反應的活性或者在反應過程中發生去官能化,這在一定程度上限制了該方法的廣泛應用(Figure 1A)。例如,硅烷化芳烴對親電試劑和親核試劑可能不穩定,烷氧基和鹵代硅烷基容易發生Si-X鍵的親核斷裂,并且硅取代基的大空間位阻可能會阻礙芳烴與催化劑的有效配位。此外,1,2-二取代烯烴的區域選擇性和非對映選擇性難以控制,這也使得烯烴氫硅烷化變得非常具有挑戰性。因此,開發新型硅基化合成方法具有重要意義。
(來源:Angew. Chem. Int. Ed.)
近日,德國明斯特大學的Christoph Schlepphorst博士和Frank Glorius教授共同開發了一種通過芳烴加氫將硅基化芳烴轉化為飽和的硅基化碳環和雜環化合物的方法(Scheme 1B)(Angew. Chem. Int. Ed., 2018, 57, 8297)。
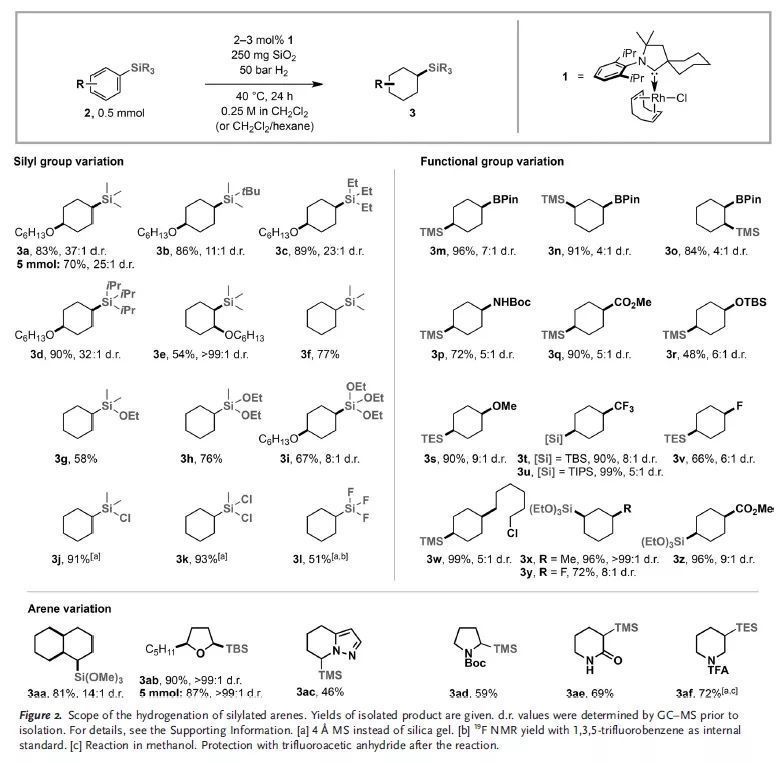
作者以課題組最近報道的多氟芳烴的加氫反應工作為基礎(Science , 2017, 357, 908),通過進一步的條件優化發現,以Rh-CAAC(1,Scheme 2)為催化劑,SiO2為添加劑,三甲基硅基芳烴的催化加氫反應可以順利高效地進行,所得產物具有優異的d.r.值(37:1)。接下來,作者對底物適用性進行了研究(Figure 2)。硅基部分空間位阻的變化對該反應沒有明顯的影響,鄰位取代的底物反應可得到具有單一非對映異構體的產物。烷氧基硅基和鹵代硅基等官能團的耐受性良好。芳環上處于硅基對位的其他官能團也具有良好的容忍性,比如硼基、Boc保護的氨基、酯基。其它吸電子基(如三氟甲基、氟)或給電子基(如甲氧基)也可以耐受。值得注意的是,該反應同樣適用于稠合芳烴和雜環芳烴。
(來源:Angew. Chem. Int. Ed.)
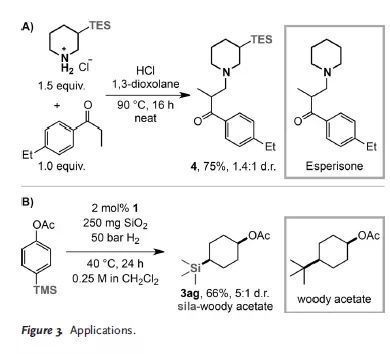
隨后,作者以產物3af和4-乙基-苯丙酮為原料,通過酸介導的曼尼希反應合成了肌肉松弛劑esperisone類似物4,為該先導化合物的結構修飾提供了一種新的方法(Figure 3B)。另外,作者結合碳-硅交換的思想,利用該反應合成了具有水果氣味的硅代鳶尾酯3ag,進一步證明了該反應的實際應用價值(Figure 3B)。
(來源:Angew. Chem. Int. Ed.)
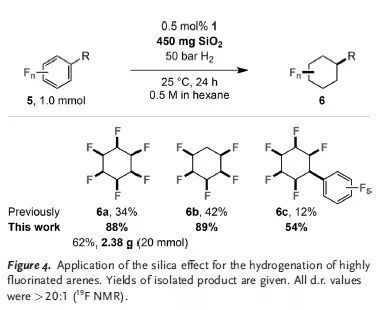
最后,作者發現使用該方法可以將多氟苯高效轉化為順式多氟環己烷,并且反應可以實現克級規模的制備。與之前報道的方法相比,該反應中的二氧化硅效應可以顯著提高反應的產率,具有明顯的優勢。
(來源:Angew. Chem. Int. Ed.)
結語:德國明斯特大學的Christoph Schlepphorst博士和Frank Glorius教授士合作開發了一種Rh-CAAC催化的硅基化芳烴的加氫反應。該反應可用來制備具有三維空間結構的硅基化飽和碳環和雜環化合物,并可用于合成藥物esperisone的類似物和具有香味的硅代鳶尾酯。








