獨腳金內酯是一種可以調節植物根部生長的植物激素,主要包括正規的獨腳金內酯、非正規的天然產物avenaol以及人工合成的GR24這三種(Figure 1)。獨腳金內酯結構的主要特點為丁醛內酯環(D環)通過乙縮醛與烯醇相連。D環可以通過非選擇性的縮醛化反應以及對所得兩個非對映異構體進行分離而得到得到。同時,金屬Pd和手性配體催化的不對稱反應也可有效地構建手性乙縮醛,但該策略的底物擴展范圍還不清楚。
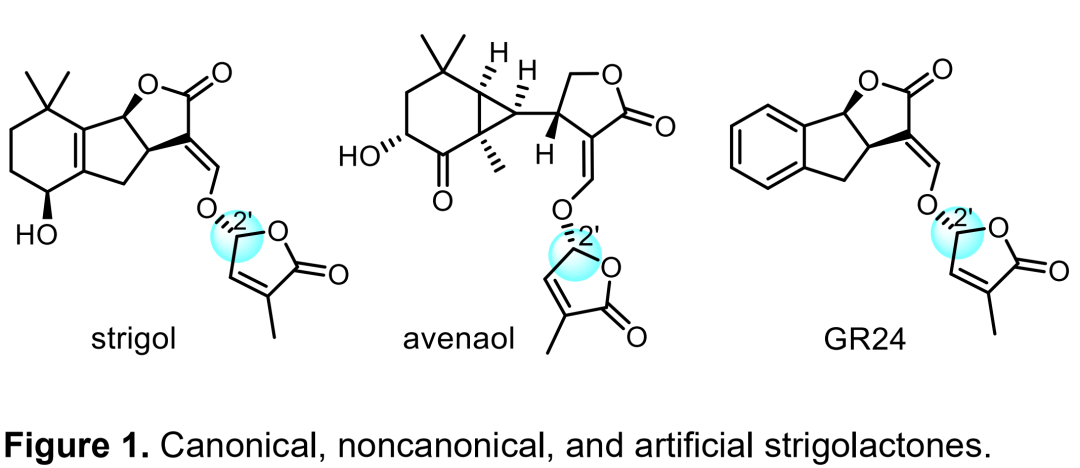
(圖片來源:Angew. Chem. Int. Ed.)
隨著時代的發展,現在已經出現了許多關于不對稱合成手性縮醛的新方法。例如,List課題組開發的手性磷酸催化分子內的不對稱縮醛反應以及非手性二醇轉化為相應的氧碳鎓陽離子與醛發生分子間的不對稱縮醛反應(Figure 2a)。但目前還沒有關于消旋烷基鹵化物通過SN2型O-烷基化策略發生不對稱縮醛反應的報道。在上述背景研究的基礎上,日本東京大學Yoshiji Takemoto、Chihiro Tsukano團隊以及匈牙利科學院Imre Pápai團隊共同報道了新型手性硫脲-季銨鹽雜化相轉移催化劑(PTC)催化非手性烯醇1通過SN2型O-烷基化策略與外消旋的γ-氯丁烯內酯2發生不對稱縮醛反應,其中2會發生動力學拆分過程(Figure 2b)。為了保證產物3的高立體選擇性,這種相轉移催化劑可以同時與親電試劑和親核試劑發生多重非共價連接。相關研究成果發表于Angew. Chem. Int. Ed.(DOI: 10.1002/anie.202002129)。
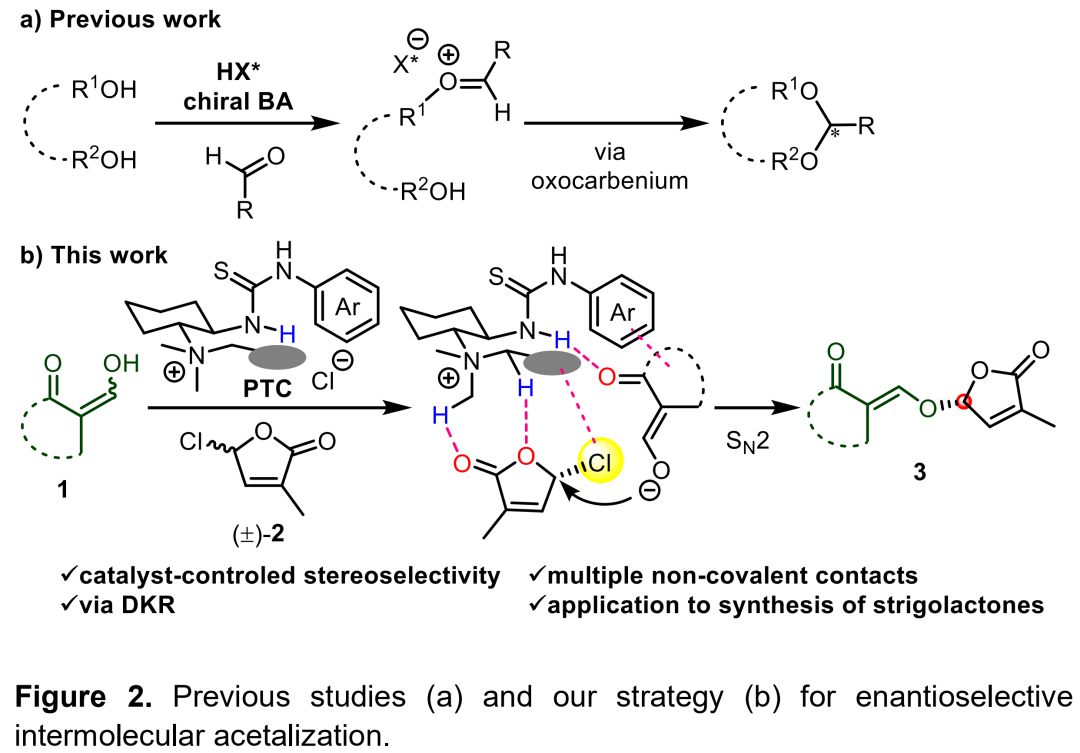
(圖片來源:Angew. Chem. Int. Ed.)
作者以烯醇1a和γ-氯丁烯內酯2為模板底物,通過對催化劑、1a和2的物料比、溶劑和堿等條件進行篩選,確定最優條件為(Scheme 1):1a和2的物料比為1:1.1,10 mol% PTC-14為催化劑,PhCl/H2O(20:1)為溶劑,2 equiv Cs2CO3為堿,在0 ℃條件下反應48 h,能以72%的收率和94:6 er得到相應產物。
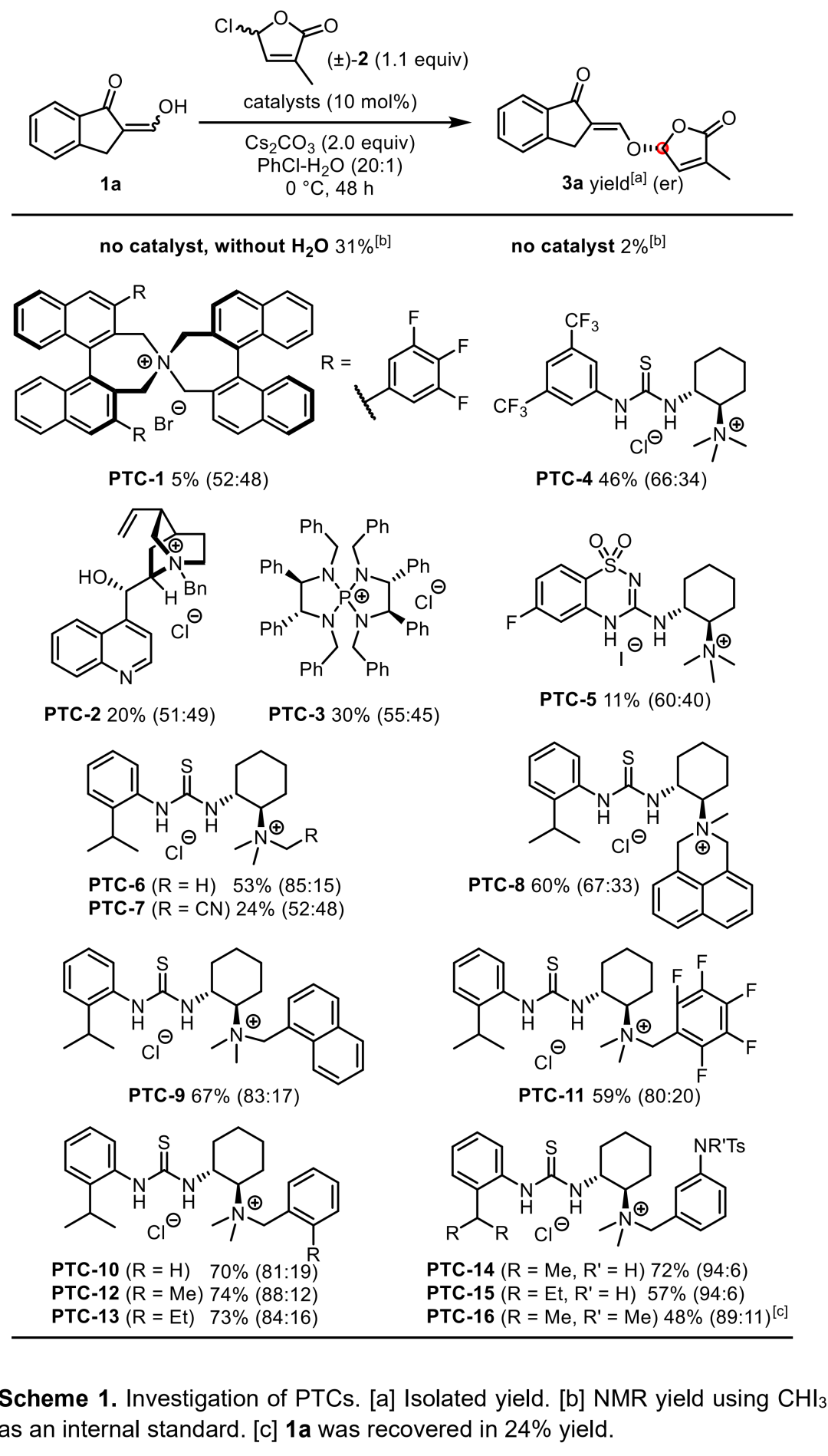
(圖片來源:Angew. Chem. Int. Ed.)
在最優反應條件下,作者對烯醇的底物范圍進行了考察(Scheme 2)。各種C5位親電取代、C6位取代以及C7位取代的烯醇均能較好地適應反應條件,以良好的收率和對映選擇性得到相應產物。當烯醇的C5位被吸電子基取代時,產物的收率有所降低,主要是因為C5位吸電子基取代的烯醇在溶劑中的溶解度會降低。非環狀的烯醇和4-溴芐醇不能適應該反應條件,相應產物的收率及對映選擇性都很低,這說明環狀烯醇對于該反應的發生尤為重要。
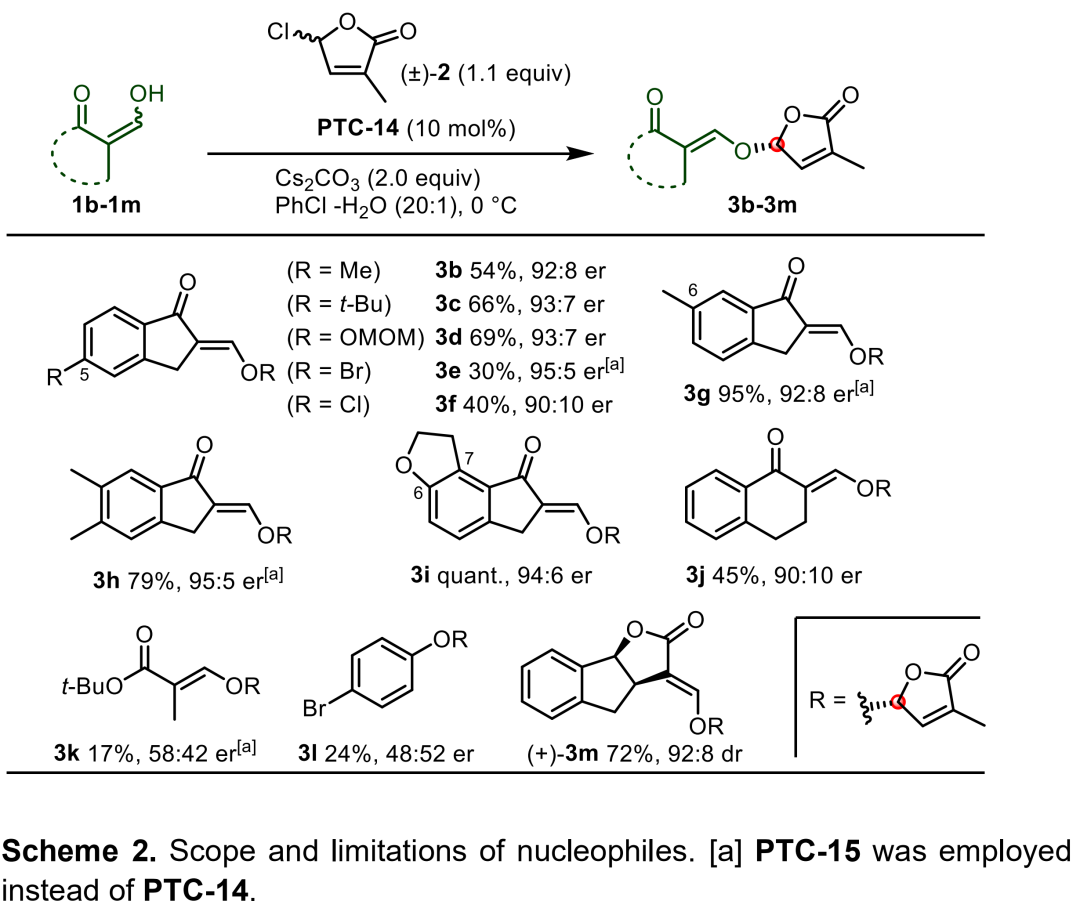
(圖片來源:Angew. Chem. Int. Ed.)
為了證明該反應的應用潛力,作者進行了一系列衍生反應(Scheme 3)。作者首先合成了1m、1n和1o,然后將這些原料轉化為各種獨腳金內酯。在最優反應條件下,1m和 1n均能較好地適應反應條件,以中等的收率和良好的對映選擇性分別得到兩種構型的(+)-GR24(3m)和(?)-ent-2'-epi-3m以及(+)-GR7(3n)和(?)-ent-2'-epi-3n。同時,1o在最優反應條件下也可轉化為3o和(?)-ent-2'-epi-3o。通過簡單的衍生反應,3o可生成天然產物avenaol(4)。
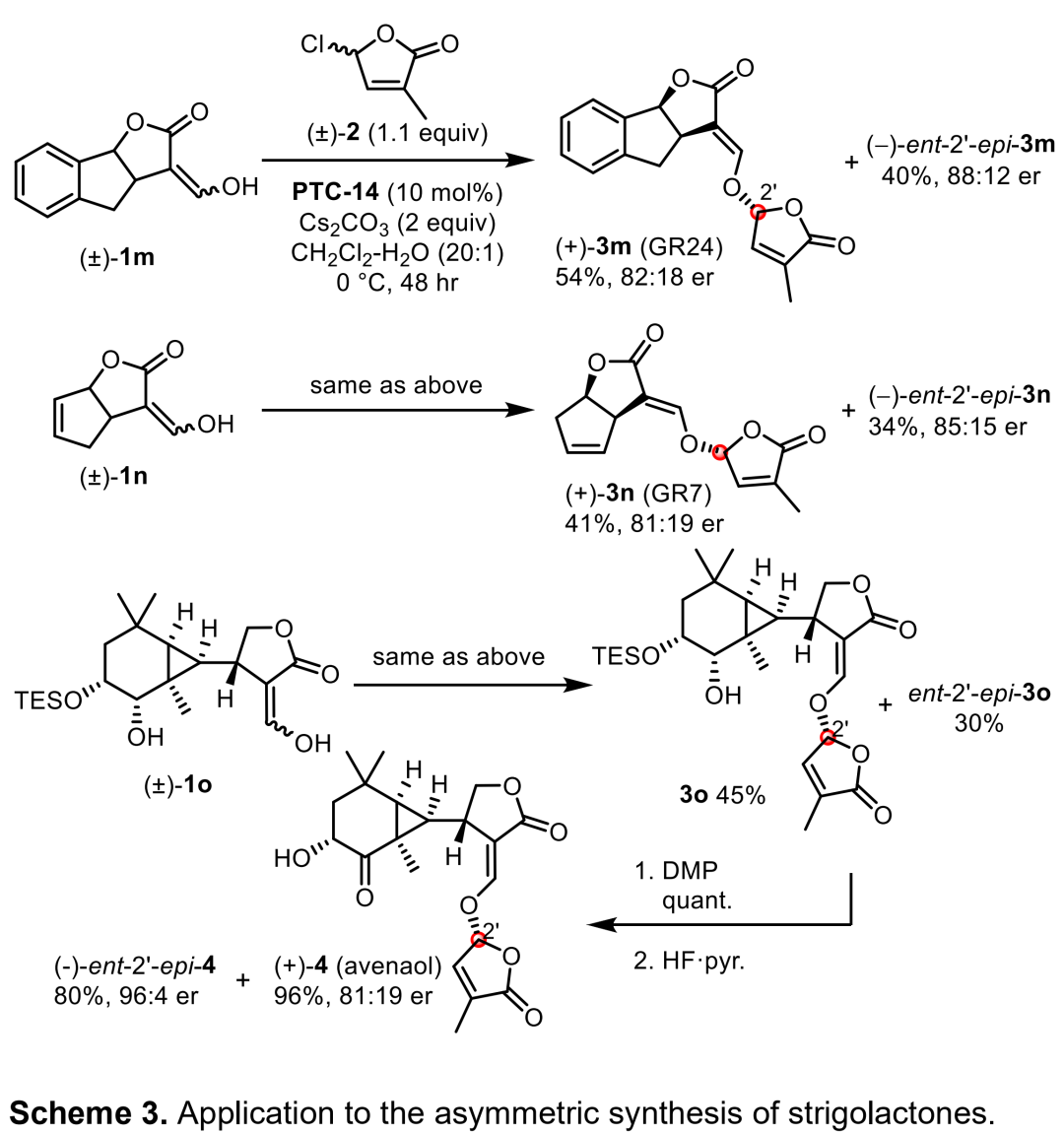
(圖片來源:Angew. Chem. Int. Ed.)
作者根據實驗結果推測了可能的反應機理:首先,由1a生成的親核烯醇en-會與陽離子催化劑cat+在水相中形成離子對中間體,然后離子對中間體cat+/en?會從水相移至有機相與γ-氯丁烯內酯2反應得到3a。同時,密度泛函理論計算(DFT)顯示烯醇化合物會優先與催化劑的鄰異丙基苯基硫脲部分相互作用,而化合物2則是由催化劑的甲苯磺酰胺和季銨鹽部分活化(Figure 3)。
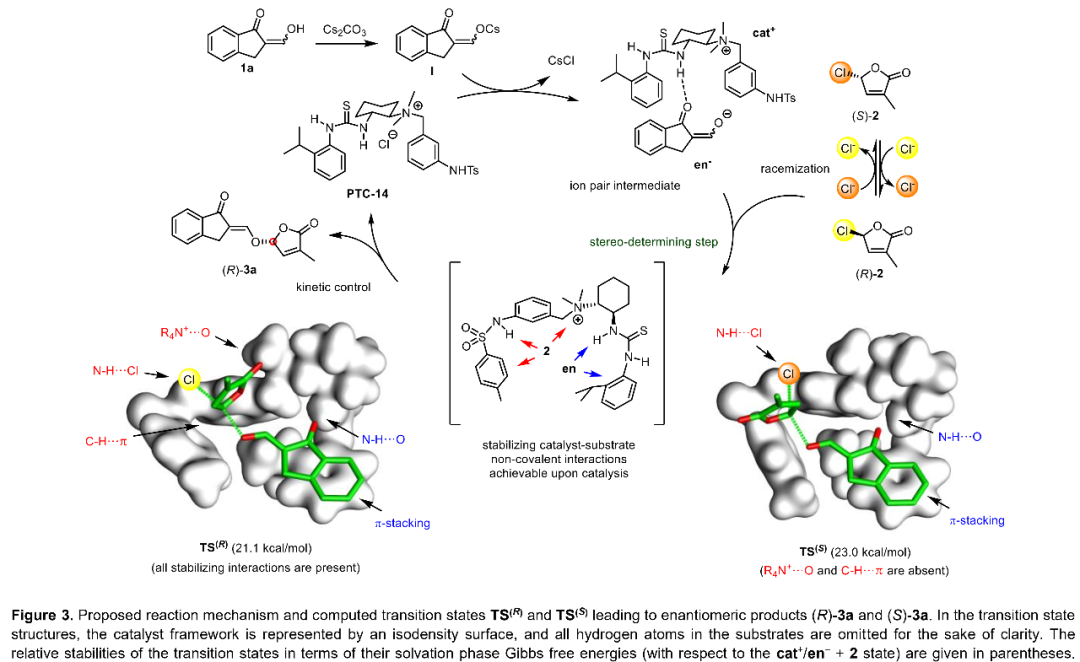
(圖片來源:Angew. Chem. Int. Ed.)
小結:日本東京大學Takemoto、Tsukano團隊以及匈牙利科學院Pápai團隊共同報道了新型手性硫脲-季銨鹽雜化相轉移催化劑催化非手性烯醇1通過SN2型O-烷基化策略與外消旋的γ-氯丁烯內酯2發生不對稱縮醛反應,其中2會發生動力學拆分過程。通過該策略還可直接合成植物激素獨腳金內酯。同時,DFT計算揭示了這種相轉移催化劑可以同時與親電試劑和親核試劑發生多重非共價連接。這是第一例有機催化SN2型分子間不對稱縮醛化反應的報道,對于有機不對稱合成的發展具有重要意義。








