分子軌道理論又稱分子軌道法(Molecular Orbital Theory)或MO法,1932年由美國(guó)化學(xué)家馬利肯(R.S.Mulliken)及德國(guó)物理學(xué)家洪特(F.Hund)提出。是現(xiàn)代共價(jià)鍵理論之一。它的要點(diǎn)是:從分子的整體性來(lái)討論分子的結(jié)構(gòu),認(rèn)為原子形成分子后,電子不再屬于個(gè)別的原子軌道,而是屬于整個(gè)分子的分子軌道,分子軌道是多中心的;分子軌道由原子軌道組合而成,形成分子軌道時(shí)遵從能量近似原則、對(duì)稱性一致(匹配)原則、最大重疊原則,即通常說(shuō)的“成鍵三原則”;在分子中電子填充分子軌道的原則也服從能量最低原理、泡利不相容原理和洪特規(guī)則。1927年,我們所熟知的價(jià)鍵理論被提出,隨后,受到洪特,馬利肯,斯萊德和John Lennard-Jones的影響,分子軌道開(kāi)始產(chǎn)生。因此,在最初的時(shí)候,分子軌道理論被稱為洪特-馬利肯理論。而“軌道”一詞的概念則是在1932年首先被馬利肯提出。到了1933年,分子軌道理論已經(jīng)被廣泛的接受,并且被認(rèn)為是一個(gè)有效而且有用的理論。事實(shí)上,根據(jù)德國(guó)物理化學(xué)家休克爾的描述,第一篇使用分子軌道理論的文獻(xiàn)是由萊納德瓊斯發(fā)表于1929年。而第一個(gè)使用分子軌道理論的定量計(jì)算文獻(xiàn)則是在1938年由庫(kù)爾森發(fā)表的使用自洽場(chǎng)理論解決氫分子的電子波函數(shù)的工作。到1950年,分子軌道徹底被定義為自洽場(chǎng)哈密頓算符的本征函數(shù),這就是分子軌道理論發(fā)展成為一個(gè)嚴(yán)謹(jǐn)科學(xué)理論的標(biāo)志。HF方法(Hartree-Fock method)是分子軌道理論的一種比較嚴(yán)謹(jǐn)?shù)奶幚矸椒ǎM管在一開(kāi)始,HF方法是用來(lái)計(jì)算原子的電子結(jié)構(gòu)的一種方法,但是在分子計(jì)算當(dāng)中,分子軌道按照原子軌道的一組基集被拓展,發(fā)展出羅特漢方程,以此為基礎(chǔ),又發(fā)展出了各種各樣的從頭算量子化學(xué)計(jì)算方法。與此同時(shí),分子軌道理論也被應(yīng)用在了一種采用了更多近似方法的半經(jīng)驗(yàn)計(jì)算當(dāng)中,被稱為半經(jīng)驗(yàn)量子化學(xué)計(jì)算方法。
軌道簡(jiǎn)介
1、原子在形成分子時(shí),所有電子都有貢獻(xiàn),分子中的電子不再?gòu)膶儆谀硞€(gè)原子,而是在整個(gè)分子空間范圍內(nèi)運(yùn)動(dòng)。在分子中電子的空間運(yùn)動(dòng)狀態(tài)可用相應(yīng)的分子軌道波函數(shù)ψ(稱為分子軌道)來(lái)描述。分子軌道和原子軌道的主要區(qū)別在于:(1)在原子中,電子的運(yùn)動(dòng)只受1個(gè)原子核的作用,原子軌道是單核系統(tǒng);而在分子中,電子則在所有原子核勢(shì)場(chǎng)作用下運(yùn)動(dòng),分子軌道是多核系統(tǒng)。(2)原子軌道的名稱用s、p、d…符號(hào)表示,而分子軌道的名稱則相應(yīng)地用σ、π、δ…符號(hào)表示。2、分子軌道可以由分子中原子軌道波函數(shù)的線性組合(linear combination of atomic orbitals,LCAO)而得到。有幾個(gè)原子軌道就可以可組合成幾個(gè)分子軌道,其中有一部分分子軌道分別由對(duì)稱性匹配的兩個(gè)原子軌道疊加而成,兩核間電子的概率密度增大,其能量較原來(lái)的原子軌道能量低,有利于成鍵,稱為成鍵分子軌道(bonding molecular orbital),如σ、π軌道(軸對(duì)稱軌道);同時(shí)這些對(duì)稱性匹配的兩個(gè)原子軌道也會(huì)相減形成另一種分子軌道,結(jié)果是兩核間電子的概率密度很小,其能量較原來(lái)的原子軌道能量高,不利于成鍵,稱為反鍵分子軌道(antibonding molecular orbital),如 σ*、π* 軌道(鏡面對(duì)稱軌道,反鍵軌道的符號(hào)上常加“*”以與成鍵軌道區(qū)別)。還有一種特殊的情況是由于組成分子軌道的原子軌道的空間對(duì)稱性不匹配,原子軌道沒(méi)有有效重疊,組合得到的分子軌道的能量跟組合前的原子軌道能量沒(méi)有明顯差別,所得的分子軌道叫做非鍵分子軌道。3、電子在分子軌道中的排布也遵守原子軌道電子排布的同樣原則,即Pauli不相容原理、能量最低原理和Hund規(guī)則。具體排布時(shí),應(yīng)先知道分子軌道的能級(jí)順序。當(dāng)前這個(gè)順序主要借助于分子光譜實(shí)驗(yàn)來(lái)確定。
線性組合原則
原子軌道組合形成分子軌道時(shí)所遵從的能量近似原則、對(duì)稱性匹配原則和軌道最大重疊原則稱為成鍵三原則。
對(duì)稱性匹配原則
只有對(duì)稱性匹配的原子軌道才能組合成分子軌道,這稱為對(duì)稱性匹配原則。原子軌道有s、p、d等各種類型,從它們的角度分布函數(shù)的幾何圖形可以看出,它們對(duì)于某些點(diǎn)、線、面等有著不同的空間對(duì)稱性。對(duì)稱性是否匹配,可根據(jù)兩個(gè)原子軌道的角度分布圖中波瓣的正、負(fù)號(hào)對(duì)于鍵軸(設(shè)為x軸)或?qū)τ诤I軸的某一平面的對(duì)稱性決定。
能量近似原則
在對(duì)稱性匹配的原子軌道中,只有能量相近的原子軌道才能組合成有效的分子軌道,而且能量愈相近愈好,這稱為能量近似原則。
軌道最大重疊原則
對(duì)稱性匹配的兩個(gè)原子軌道進(jìn)行線性組合時(shí),其重疊程度愈大,則組合成的分子軌道的能量愈低,所形成的化學(xué)鍵愈牢固,這稱為軌道最大重疊原則。在上述三條原則中,對(duì)稱性匹配原則是首要的,它決定原子軌道有無(wú)組合成分子軌道的可能性。能量近似原則和軌道最大重疊原則是在符合對(duì)稱性匹配原則的前提下,決定分子軌道組合效率的問(wèn)題。

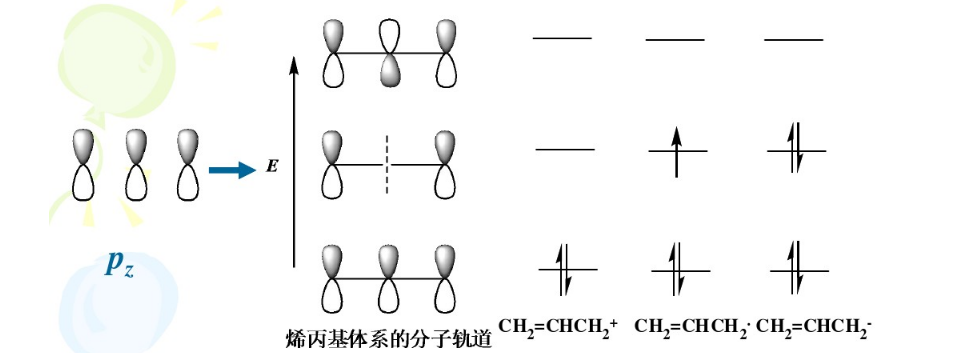
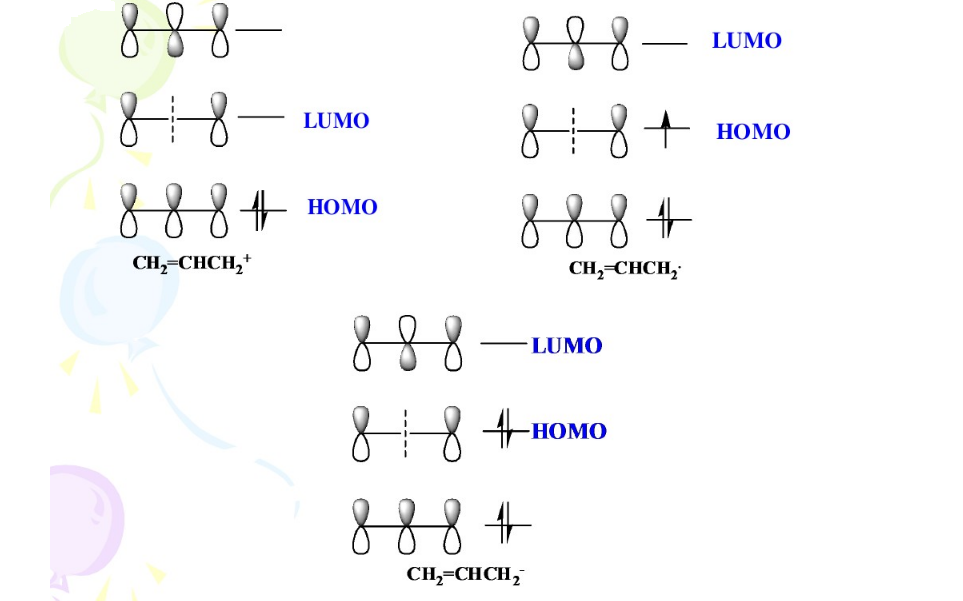
前線軌道理論,是一種分子軌道理論,是日本理論化學(xué)家福井謙一賴以成名的理論,這一理論將分子周圍分布的電子云根據(jù)能量細(xì)分為不同能級(jí)的分子軌道,福井認(rèn)為有電子排布的,能量最高的分子軌道(即最高占據(jù)軌道HOMO)和沒(méi)有被電子占據(jù)的,能量最低的分子軌道(即最低未占軌道LUMO)是決定一個(gè)體系發(fā)生化學(xué)反應(yīng)的關(guān)鍵,其他能量的分子軌道對(duì)于化學(xué)反應(yīng)雖然有影響但是影響很小,可以暫時(shí)忽略。HOMO和LUMO便是所謂前線軌道。
福井謙一提出這一理論,它的依據(jù)是:在分子中,HOMO上的電子能量最高,所受束縛最小,所以最活潑,容易變動(dòng);而LUMO在所有的未占軌道中能量最低,最容易接受電子,因此這兩個(gè)軌道決定著分子的電子得失和轉(zhuǎn)移能力,決定著分子間反應(yīng)的空間取向等重要化學(xué)性質(zhì)


原子位置在親電或親核取代反應(yīng)的相對(duì)活性是一個(gè)重要的問(wèn)題。已經(jīng)提出了各種理論指標(biāo),如電荷密度分布,定域能方法等。前線軌道理論認(rèn)為,最高已占分子軌道上的電子在各個(gè)原子上有一定的電荷密度分布,這個(gè)分布的大小次序決定親電試劑進(jìn)攻各個(gè)原子位置的相對(duì)難易程度,即親電反應(yīng)最易發(fā)生在HOMO最大電荷密度的原子上 。
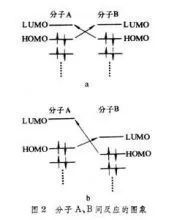
對(duì)于兩個(gè)分子A和B間的反應(yīng),前線軌道理論給出的圖像見(jiàn)下圖。即分子 A和 B的HOMO中的電子分別流向?qū)Ψ降奈凑糒UMO,從而引起化學(xué)鍵的生成和斷裂,發(fā)生化學(xué)反應(yīng)。只有分子A(或B)的HOMO與分子B(或A)的LUMO的能量比較接近,對(duì)稱性也互相匹配時(shí),才容易發(fā)生電子流動(dòng),圖2a為分子A和B相同時(shí)的情形,圖2b為A和B不相同時(shí)以A的HOMO中的電子流向B的LUMO為主的情形 。著名的分子軌道對(duì)稱守恒原理也可借助于前線軌道理論加以闡明。必須指出,前線軌道理論不僅適用于π軌道,也適用于σ軌道,因此它在有機(jī)化學(xué)、無(wú)機(jī)化學(xué),以及表面吸附與催化、量子生物學(xué)等領(lǐng)域都有應(yīng)用。
本文內(nèi)容轉(zhuǎn)自:
一、百度百科分子軌道理論:https://baike.baidu.com/item/%E5%88%86%E5%AD%90%E8%BD%A8%E9%81%93%E7%90%86%E8%AE%BA/10600165?fr=aladdin
二、百度百科前線軌道理論:https://baike.baidu.com/item/%E5%89%8D%E7%BA%BF%E8%BD%A8%E9%81%93%E7%90%86%E8%AE%BA/7055235?fr=aladdin
三、高等有機(jī)化學(xué)課件,謝斌教授。















