酮的α-烷基化是一種生成C-C鍵的常見合成手段也已在合成化學中廣泛使用。通過酮的去質(zhì)子化所形成高度親核的堿金屬烯醇鹽,經(jīng)由SN2途徑與鹵代烷反應即可實現(xiàn)這樣的反應。不過,由于金屬烯醇鹽的強堿性和親核性質(zhì)卻也限制了許多官能團的可容忍范圍,導致化學選擇性較差的問題。因此,尋求避免使用強堿金屬烯醇鹽的溫和替代品也是這種化學的目標。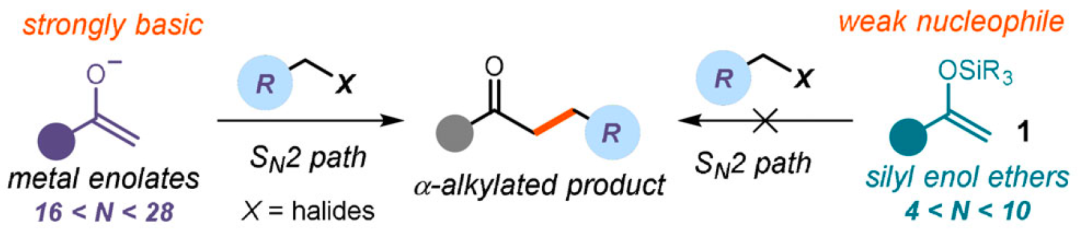
圖片來源:Angew. Chem. Int. Ed.
近期,ICIQ的Paolo Melchiorre教授在Angew. Chem. Int. Ed.上報道了可見光催化的酮α-烷基化反應,即可作為替代方案之一。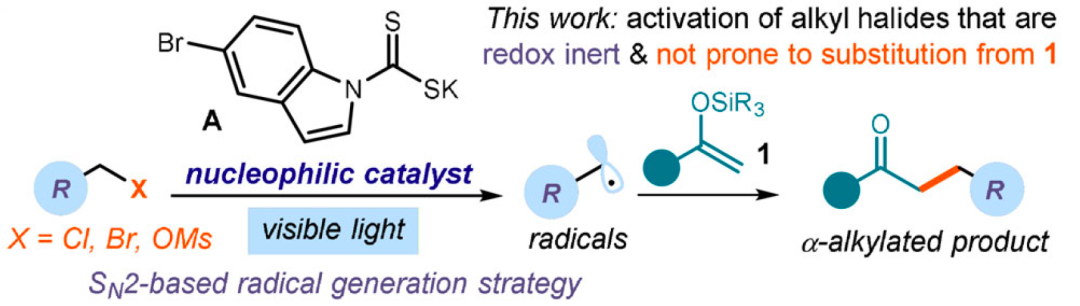
圖片來源:Angew. Chem. Int. Ed.
該方法利用了親核型有機催化劑可將烷基鹵化物進行SN2反應和藍光照射下產(chǎn)生自由基的能力,將所得的自由基中間體(II)與甲硅烷基烯醇醚結合,再經(jīng)電子轉(zhuǎn)移及脫硅烷以獲得酮α-烷基化的產(chǎn)物。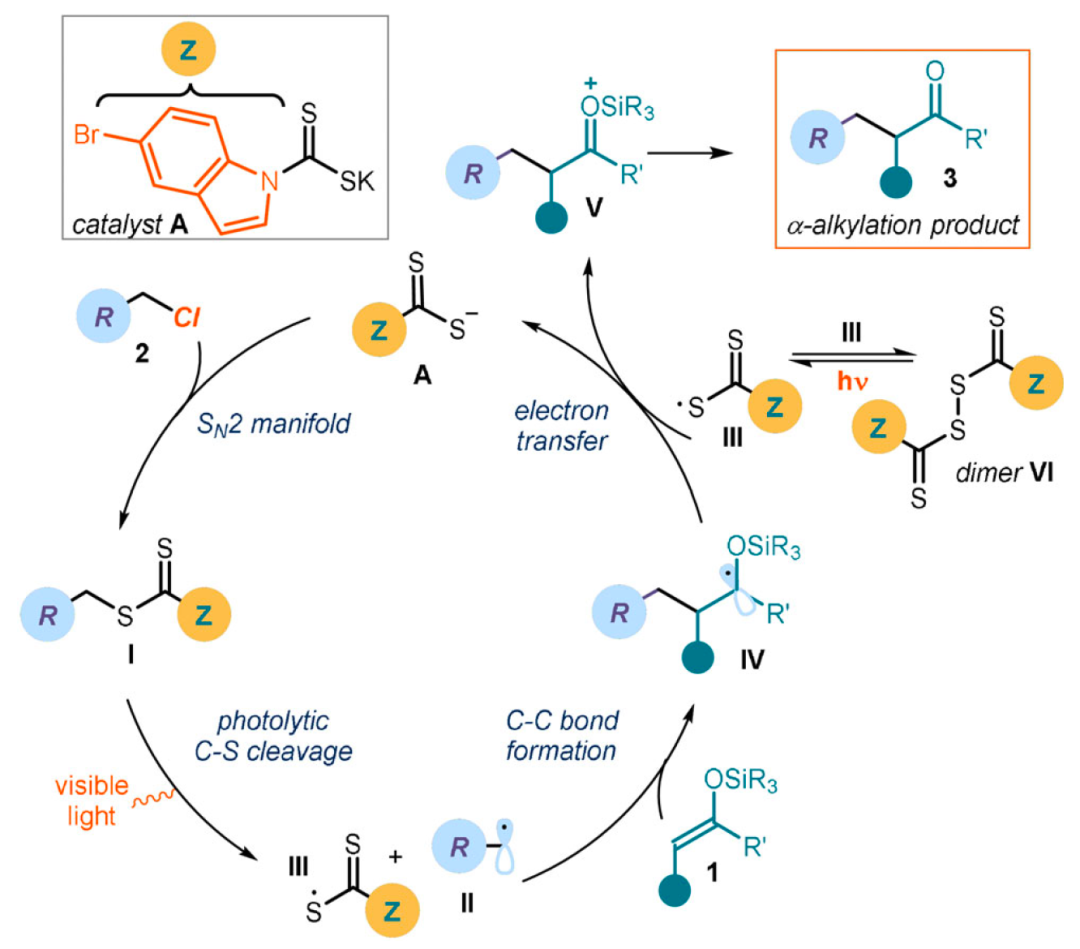
圖片來源:Angew. Chem. Int. Ed.
甲硅烷基烯醇醚是穩(wěn)定的烯酸酯等效物,易于合成和處理。且這些化合物已廣泛用于親核加成化學,如醛醇、邁克爾和曼尼希型方法等。該反應可實現(xiàn)與過去以陰離子策略不兼容的官能團進行酮的官能化,并維持溫和的反應條件。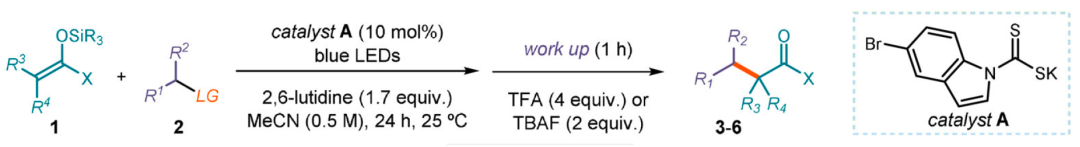
圖片來源:Angew. Chem. Int. Ed.
另外,該方法的氧化還原中性性質(zhì)也使其與手性的金雞納酮伯胺催化劑相容,使反應可適用于酮的不對稱催化α-烷基化反應的開發(fā)。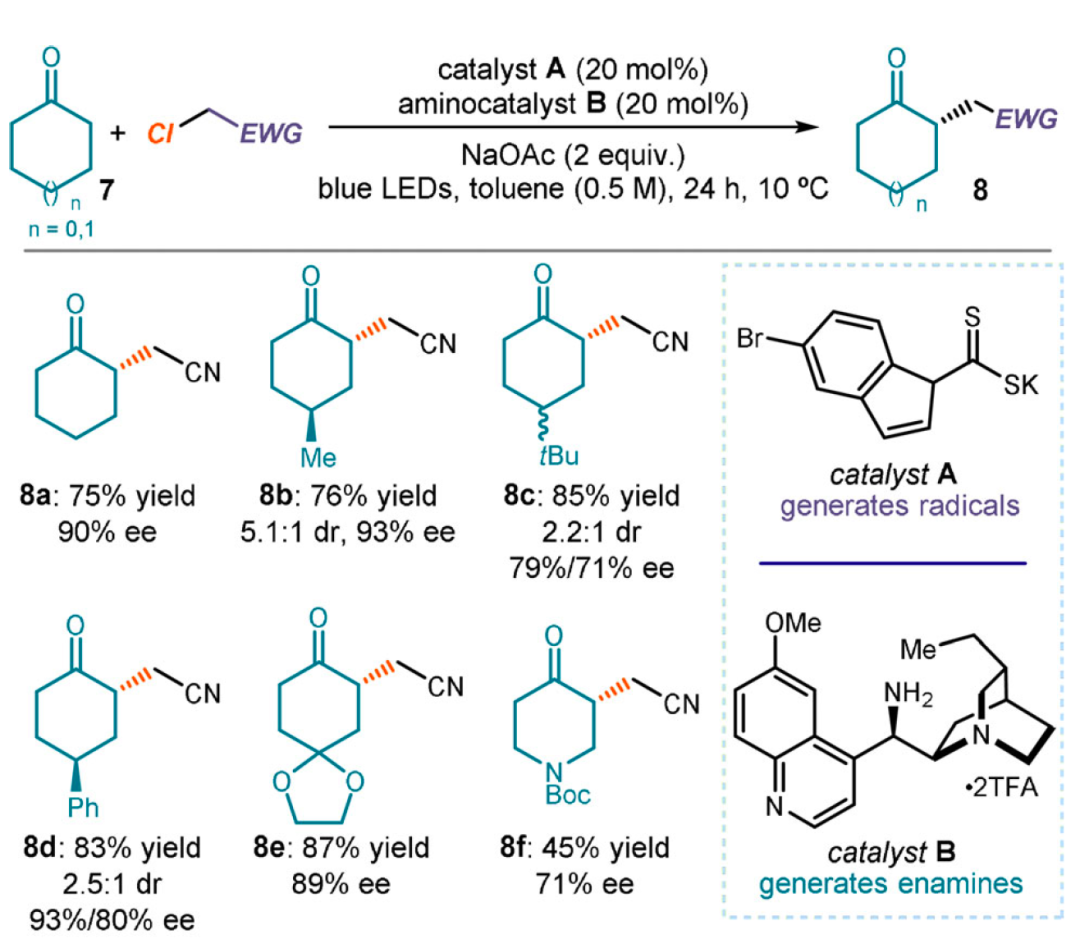
圖片來源:Angew. Chem. Int. Ed.
參考文獻:A Photochemical Organocatalytic Strategy for the a-Alkylation of Ketones by using Radicals
DOI: 10.1002/anie.201915814
原文作者:Davide Spinnato, Bertrand Schweitzer-Chaput, Giulio Goti, Maksim Oseka, and Paolo Melchiorre*













