第一作者:吳立波
通訊作者:何錦韋
通訊單位:新加坡國立大學
論文DOI:10.1021/acsnano.4c18818
隨著綠色低碳發展日益成為全球共識,海水這一取之不盡、用之不竭的自然資源,正逐漸被賦予新的使命--成為綠色化學與能源轉型的重要推手。相比淡水,海水不僅儲量巨大,更因其離子種類豐富而具備多元利用潛力。通過特定的電化學反應和裝置設計,海水不僅可以用于制氫,還可產出氯化物、鈉、鎂、碳基化合物等多種高價值燃料與化學品。盡管近年來關于海水制氫的研究逐漸升溫,但圍繞更廣泛海水電化學反應的系統探索仍相對滯后。近日,新加坡國立大學何錦韋課題組系統梳理了海水電化學用于綠色燃料與化學品制造的前沿成果。該綜述以Advancing Seawater Electrochemical Reaction for Fuel and Chemical Production為題,發表于ACS Nano (ACS Nano 2025, 19 11 10779-10795. DOI: 10.1021/acsnano.4c18818)。文章總結了海水電化學反應的基本原理、關鍵挑戰與研究進展,重點展示了海水在氫氣之外的高價值產物制備中的應用前景,關注創新的電化學反應機制、先進催化劑開發以及集成系統設計。綜述呼吁未來應深化催化劑和電解系統研發、推進真實海水條件下的測試、優化產物分離與系統能耗評估,加快推動海水資源在綠色能源與化學品制造中的可持續轉化,為全球碳中和注入新動力。
一、引言
海水作為地球上最豐富的資源之一,憑借其化學成分多樣性,正成為綠色化學和能源轉型的重要突破口。盡管其在反應過程中存在如腐蝕、副反應、雜質沉積等挑戰,海水電解制氫仍廣受關注,成為當前研究熱點。從更廣闊的視角看,海水更具備作為多種化學反應原料或中間體的潛力。結合合適的電化學反應,海水可實現從清潔燃料到高附加值化學品的多元產出(圖1)。為此,本綜述從催化劑開發、電解系統設計到天然海水環境下的代表性轉化案例,全面梳理海水電化學的最新進展,并展望其未來發展路徑,旨在推動海水資源在電化學領域的深度利用。本綜述不僅聚焦于催化劑的開發與優化,還強調集成化系統設計在提升反應效率與應對海水電化學挑戰中的關鍵作用。
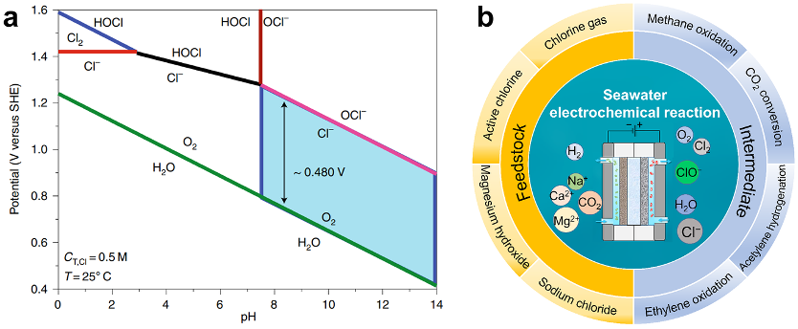
圖1. (a) 在0.5 M NaCl電解液中,不同pH條件下H2O/O2與Cl?/Cl2/HOCl/ClO?氧化還原體系的Pourbaix圖。(b)海水電化學反應生產多種燃料與化學品。
二、海水電化學反應:成分、原理與挑戰
理解海水的主要組成是推動其可持續電化學利用的基礎。海水中含有種類豐富的離子和溶解氣體。其中,氯離子(Cl?)濃度最高,約為19.162 g/kg,廣泛應用于化學合成和消毒劑制造;鈉離子(Na+)濃度為10.679 g/kg,是最主要的陽離子,可用于制備燒堿及鈉基化工品。鎂離子(Mg2+,1.278 g/kg)廣泛應用于輕質合金、醫藥及精細化工;鈣離子(Ca2+,0.41 g/kg)常用于水泥與紙漿漂白工藝;而鉀離子(K+,0.395 g/kg)則在有機合成、洗滌劑和肥皂生產中有重要用途。此外,海水還含有溴離子(Br?)、鍶離子(Sr2+)、氟離子(F?)和鋰離子(Li+)等微量元素,盡管濃度較低,但具有較高經濟價值。海水中還溶解有大量氣體,其中海水對CO2的吸收在當前實現“碳中和”目標中具有日益突出的作用。海水不僅可作為電化學反應的原料來源,其豐富的離子種類還能在電催化過程中作為活性中間體參與反應。要充分挖掘海水在燃料與化學品生產方面的潛力,需要超越傳統的電解海水反應思維,充分利用海水中的H+、OH?、Cl?等中間物質與溶解鹽發生反應,推動海水電化學發展。
三、海水作為原料用于燃料和化學品合成
3.1 氯離子相關反應
次氯酸(ClO?)是一種高效消毒劑,廣泛應用于廢水和壓載水處理。傳統上,這類消毒劑是通過氯堿工藝電解高濃度氯化鈉溶液制備。近年來,研究者開始嘗試利用海水電合成次氯酸。Zhao等人提出了一種基于非貴金屬Fe摻雜Ti4O7陽極的方案,利用天然海水高效合成ClO?(圖2a)。該電極展現出與商業陽極相當的高活性(圖2b、c),并可有效抑制電極鈍化。電化學性能測試及氯析出機制研究表明,Fe的引入使得催化劑以低于OER的過電位實現Cl?活化,提升反應選擇性。生成的ClO?可在5分鐘內快速滅活海水中的常見致病菌,展現了其在船舶壓載水處理中的應用潛力。盡管通過設計催化劑可以降低氯化物氧化反應過電位,但電解海水制氫的整體電壓仍然偏高,其主要受限于HER反應過程中的水解步驟所需額外能量,以及海水本身較低的導電性(圖2d)。Zhu等人提出了一種酸-鹽水混合電解系統,用于高效共電合成ClO?和H2。該系統使用雙功能TiRu/Ti電極,陽極電解液為1 M NaCl,陰極電解液為0.5 M H2SO4,通過雙極膜隔開(圖2e)。該設計顯著降低能耗,僅需42.27 kWh即可產出1 kg氫氣,比直接鹽水電解降低了27.7%的能耗(圖2f)。酸化的海水陽極液不僅抑制了Ca/Mg鹽類沉淀,還促進了次氯酸生成,適合用于快速殺菌消毒及農業應用(如豌豆芽育苗)。過氧化氫(H2O2)作為一種用途廣泛的氧化劑,目前主要通過蒽醌氧化法(AOP)生產,不僅工藝復雜,還依賴氫氣等原料。Zhao等人開發出一種基于單原子Co催化劑的流動電解池系統,在陰極通過兩電子氧還原反應(ORR)生成H2O2,陽極采用RuO2催化Cl?氧化生成Cl2。海水產生的氯氣也可用于鐵(Fe)生產,為減少鋼鐵工業碳排放提供新路徑。Noble等人提出一種低溫電解方法,通過Fe2O3與高濃度NaCl海水電解耦合,同時制備高純度Fe、NaOH與Cl2氣體,實現零碳排放。他們進一步構建了一個流動電解槽,在100 mA cm?2電流密度下可穩定運行4小時。該系統Fe生成法拉第效率達84%,純度超過95 wt%。需要注意的是,氯氣是一種高毒性氣體,其研究過程必須嚴格控制安全風險。
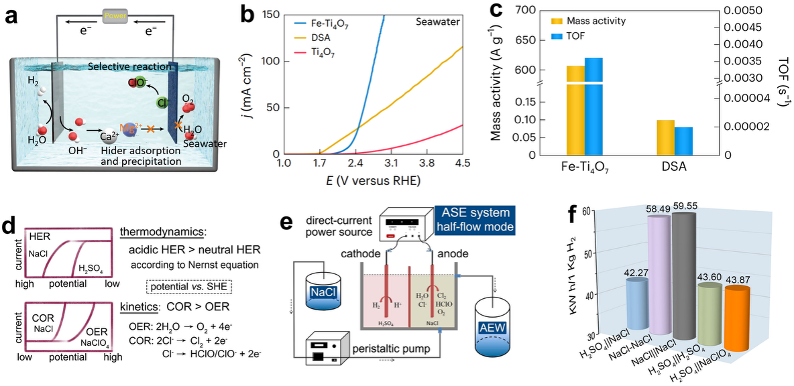
圖2.(a)采用Fe- Ti4O7陽極進行海水電解制備活性氯的示意圖。(b) 在無緩沖海水中,Ti4O7與Fe-Ti4O7陽極用于氯析反應的線性掃描伏安極化曲線對比。(c) Fe- Ti4O7陽極與商業DSA陽極在活性氯生成反應中的質量活性與周轉頻率對比。(d) 酸-鹽水混合電解體系設計的理論基礎。(e) 實時聯產氫氣與活性氯的酸-鹽水混合電解系統結構模型。(f) 不同電解體系獲得1.0 kg氫氣所需電能消耗對比。
3.2 鈉離子相關反應
除了與Cl?相關的活性氯與氯氣產物,海水中豐富的Na?可以用來生成氯化鈉或氫氧化鈉,進一步提升海水電化學經濟效益。例如,Li等人引入“同離子效應”策略,實現了氫氣、氧氣與氯化鈉晶體的三聯產(圖3a)。該策略的原理為:溶液中陽離子與陰離子濃度的乘積存在溶度積平衡,提高一種離子濃度會降低其反離子的溶解度。他們在經過處理的海水中加入6 M NaOH(含Na?),顯著降低NaCl(含Cl?)的溶解度(圖3b)。同時,高濃度OH?有利于析氧反應(OER),抑制析氯副反應。使用NiCoFeP雙功能催化劑,該系統在500 mA cm-2電流密度下可穩定運行超過100小時。此外,Du等人提出了一種膜法氯堿電解技術,從海水淡化濃鹽水中同步制取NaOH、H2和Cl2(總反應:2NaCl + 2H2O → 2NaOH + H2+ Cl2)(圖3c)。該流程首先通過納濾去除海水中的硫酸鹽和硬度離子,然后通過滲析濃縮、蒸發或機械壓縮使其達NaCl飽和,最后酸化后引入膜電解槽。在陽極,Cl?被氧化為Cl2氣體,水也發生部分氧化;陰極則產生H2氣體和OH?,后者與Na+結合形成NaOH。
3.3 鈣離子相關反應
碳酸鈣作為造紙、塑料和建材等行業的重要原料,其制備不僅具備產業價值,更為海水中CO2捕集與資源化利用提供了新途徑,可謂“一石二鳥”。Sharifian等人開發了一種原位雙極膜電滲析(BPMED)系統,將海水中溶解的無機碳轉化為固態碳酸鹽(圖3d)。該系統中,CO2首先與OH?反應生成HCO3?,再進一步形成CO32?,最終與天然海水中的Ca2+結合沉淀為CaCO3。
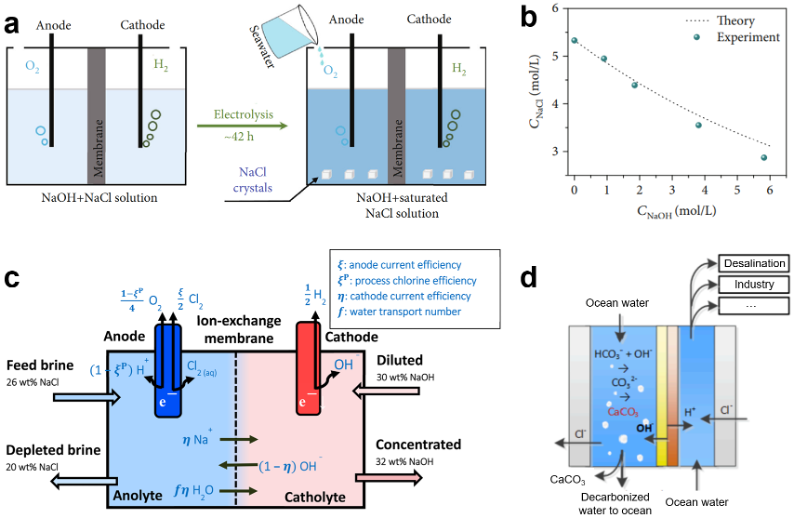
圖3.(a)在海水電解過程中引入“同離子效應”,以提升電化學性能,并實現三重產物聯產。(b)在不同初始NaOH濃度條件下,海水電解過程中NaCl濃度的變化趨勢。(c)典型氯堿工藝反應單元的結構示意圖。(d)采用堿化路徑實現CO2礦化處理的反應示意圖。
3.4 鎂離子相關反應
氫氧化鎂廣泛應用于阻燃劑、中和劑、食品添加劑等領域,開發高效、低成本的海水電解提鎂方法具有重要意義。Yi等人利用Pt-NiCu合金在HER過程中生成OH?,使其與海水中的Mg2+反應沉淀為Mg(OH)2(圖4a-d)。采用Pt-NiCu陰極和IrO2-Ti陽極的膜電解槽可在100 mA cm?2下穩定運行100小時,產出高達19.07 g、純度>99%、粒徑約20 μm的Mg(OH)2,鎂提取效率達44.6%。此外,Liang等人通過電還原天然海水,利用自清潔Pt/C碳基電極制備了Mg(OH)2納米片(圖4e-g)。該電極由K2PtCl6處理后木材高溫退火制得,具有規則孔隙結構與外部水流擾動設計,可有效帶走OH?與沉淀,避免電極鈍化。在?200 mA下,Mg(OH)2生成速率達~0.345 g h?1cm?2。
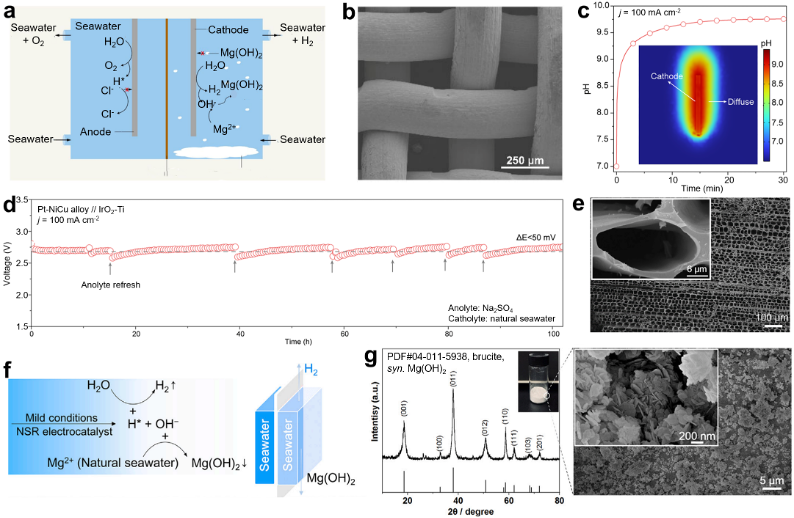
圖4.(a)通過海水電解同步制備氫氣和氫氧化鎂的反應示意圖。(b) Pt-NiCu合金催化劑的SEM圖像。(c) 在100 mA cm?2電流密度下,電極附近區域的pH分布的COMSOL仿真結果。(d) 在100 mA cm?2電流密度下,天然海水電解裝置的穩定性測試結果。(e) 不同放大倍率下Pt/碳電極頂部表面的SEM圖像。(f) 僅依靠電力驅動的聯產氫氧化鎂與氫氣的電解系統示意圖。(g) 所收集沉淀物的XRD圖譜與SEM表征圖像。
四、海水作為中間介質用于燃料和化學品合成
除了作為原料外,海水還可作為電化學反應中的中間介質,參與多種電化學反應。與淡水相比,海水富含鹵素離子,能夠為電化學反應創造更有利的微環境,有助于促進O?H和C?H鍵的活化,或者形成鹵素中間體以提高反應選擇性。
4.1 氯促進的甲烷氧化
甲烷是石油開采中的重要副產物,是強效溫室氣體,其溫室效應是CO2的數十倍。因此,開發可再生能源驅動的甲烷轉化路徑,有利于石油行業減碳。由于甲烷C–H鍵能高、極性弱,溫和條件下難以活化。針對這一挑戰,Wang等人提出了一種以CoNi2Ox催化劑為核心的電催化策略,利用,CER產生*Cl中間體,實現甲烷向甲醇(CH3OH)的高效轉化。相比傳統OER路徑,CER可在更低電位下激活C–H鍵,且通過CH3Cl中間體的釋放,抑制過氧化副反應,顯著提升產物選擇性。
4.2 鈉促進的乙炔加氫
傳統乙炔加氫制乙烯依賴高溫高壓工藝,而電催化路徑則以水為質子源,提供更綠色的替代方案。Qiao課題組發現,Na+離子可通過調控界面水結構,促進水解并加速*H中間體生成,從而提高加氫效率與產物選擇性。在濃海水電解液中,利用Cu基催化劑實現了高達95.1%的乙烯法拉第效率和0.6 A cm?2的電流密度。基于此,他們構建了一體化系統:先電解海水制氫,繼而電催化乙炔加氫,實現氫氣與乙烯協同生成。該系統在連續32小時運行中,乙烯和氫氣產率分別達約7.47和7.58 mmol h?1cm?2。
4.3 氯促進的乙烯氧化
近年來,氯中介電化學氯醇化受到關注。Chung等利用Co3O4陽極在模擬海水中電催化乙烯氧化,優先生成2-氯乙醇(C2H5ClO),后續加熱轉化為環氧乙烷或乙二醇。他們發現,天然海水中的Mg2+有助于提升C2H5ClO的選擇性。在過濾海水中法拉第效率達71%,顯著優于NaCl溶液(41%)。另一項研究由Huang等人提出,他們利用PEM電解槽在酸性海水中進行乙烯氧化,發現氯離子氧化速率顯著提高,抑制了*OH吸附,進而降低了副產物C2H6O2的生成,提高了C2H5ClO的產率。
4.4 海水介導二氧化碳轉化
將CO2捕集與電化學轉化整合,并以海水為電解質,是具有潛力的研究方向。Digdaya等人提出了一種集成系統,結合雙極膜電滲析(BPMED)和氣相CO2還原反應電解槽。該BPMED模塊由兩個海水腔和兩個可逆氧化還原對溶液腔組成,中間以陽離子交換膜隔開,外部配有兩個電極。酸化海水經三段膜接觸器,通過真空泵釋放溶解CO2,實現71%捕集效率。捕集后的CO2氣體直接輸送至Cu或Ag催化劑構成的CO2RR電解槽進行還原。此外,海水還可在CO2RR中提供電子和質子作為有效電解質。例如,Nakata等人在摻硼金剛石電極上,以海水為電解液將CO2電還原為甲醛(HCOH),不僅提高高附加值產物的選擇性,還抑制H2的生成。鑒于海水富含Cl?及具備一定碳容量,Tan等人提出在海水電解中實現Cl2與CO的協同電合成,反應路徑為:3CO2 + 2NaCl + H2O → CO + Cl2 + 2NaHCO3,副產物為碳酸氫鈉。Lee等人發現,海水CO2RR過程中,碳酸鈣沉積會覆蓋催化劑表面并降低活性位點。為解決該問題,他們構建了一個自驅動CO2電解系統,將Mg陽極與納米孔Ag陰極耦合形成原電池。Mg在陽極自發氧化生成Mg2+,Ag+在陰極被還原為金屬Ag,同時驅動CO2電還原生成CO,有效提升反應效率并避免催化劑中毒。
五、展望
海水的廣泛利用不僅能緩解水資源壓力,還為綠色電化學反應提供了新的可能性和更廣闊的發展前景。因此,深入開展海水電化學研究具有重要的科學意義和潛在的產業價值。盡管該領域已取得一定進展,但仍面臨多項科學和技術挑戰。以下幾方面是推動海水資源電化學利用進一步發展的關鍵問題:
5.1. 通過創新的電化學反應與系統設計,進一步拓展海水利用潛力
海水在燃料與化學品合成方面仍有較大探索空間。例如,借助合適的催化劑選擇與系統設計,海水電化學反應有望實現高純度有機物的合成。為此,需要通過系統性研究與創新性反應路徑開發,突破現有的技術瓶頸。因此,研究重心不應僅局限于優化現有反應的催化劑性能,還應積極探索新型電化學反應路徑與系統,從而拓展海水利用的方式與邊界。
5.2. 設計高效催化劑與電解系統,并在真實海水中評估性能
推動海水電化學反應規模化應用的關鍵在于開發高效催化劑與先進電解系統。一方面,優異的催化劑應具備良好的抗腐蝕性能、高選擇性與低能耗;合理的設計可以將沉積副產物轉化為可利用資源,提升系統整體效率。另一方面,電解器的研發是實現工程化部署的基礎。需特別強調的是,在真實海水環境中進行測試,是確保評估結果準確與技術可行性的必要步驟。相比于模擬海水體系,天然海水成分更為復雜,離子種類多樣,對催化劑和系統構成更大挑戰。因此,應在淡水、模擬海水與真實海水條件下開展對比測試,深入揭示復雜離子與雜質之間的協同或競爭效應對性能的影響,提升系統適應性。
5.3. 注重產品純度、分離效率、系統經濟性與應用價值
在海水電化學反應合成燃料與化學品的研究中,產物的高效分離與純化始終是一項關鍵挑戰。對于氣態產物和部分固態產物,可通過逸出或離心等方式實現收集。然而,對于在海水中仍具一定溶解度的液態或固態高純度化學品,其提取和純化過程則面臨更高復雜性。因此,有必要進一步優化現有的海水電解技術與裝置,開發面向特定產物的精準調控體系。同時,還應注重提升整體反應效率,確保系統具備良好的經濟性與可推廣性。
5.4. 合理考量海水電化學反應的必要性與適用性
并非所有電化學反應都適合采用海水作為電解液。在眾多已研究的體系中,氫氣制備和二氧化碳還原反應因其在可再生能源利用與碳中和戰略中的重要性,是具有前景的研究方向。此外,隨著鋰電池需求日益增長,從海水中選擇性提取鋰元素將成為綠色、可持續的資源獲取方式,鋰的電化學提取也被視為關鍵方向。鈾等關鍵元素的電化學提取也受到關注,盡管吸附法仍是目前主流,電化學策略正在成為一種有前景的新選擇。此外,海水電化學在污染物轉化(如塑料降解)方面同樣具有潛力,相關反應路徑及產物機制仍有待深入研究。總體而言,海水憑借其復雜而豐富的化學組成,在特定條件下可用于高效生成能源與材料,并協同實現環境治理。在構建海水電化學反應體系時,應全面評估其必要性與可行性,確保實現科學性與應用價值的協同提升。
通訊作者簡介:
何錦韋(HO Ghim Wei)目前是新加坡國立大學教務長講座教授,電氣與計算機工程系、材料科學與工程系雙聘教授,英國皇家化學學會會士。于劍橋大學取得博士學位,2014年被授予歐萊雅聯合國教科文組織女性科學獎。其領導的可持續智能系統實驗室(Sustainable Smart System Lab)依托多學科研究團隊,長期致力于納米能源系統的基礎和應用研究,探索其在能源、環境、電子和醫療保健領域的交叉應用,如光催化、光熱海水淡化、太陽能機電一體化、綠色能源與柔性傳感器件等。截止目前,課題組已在Nature、Nature Reviews Physics、Nature Water、Nature Communications、Science Advances、Joule、Advanced Materials、Energy & Environmental Science、Materials Today和IEEE系列等國際一流期刊發表論文200多篇。課題組所培養的博士、博士后中多人在“雙一流”(985/211)、省部高校任職。目前受邀擔任Journal of Materials Chemistry A、Materials Advances和EcoEnergy的副主編。








