分享一篇發表在Nature Biotechnology上的文章,文章的標題是Antibody–bottlebrush prodrug conjugates for targeted cancer therapy。本文的通訊作者是來自麻省理工學院的Jeremiah A Johnson教授。
抗體偶聯藥物(Antibody-Drug Conjugates, ADCs)是一類將單克隆抗體的靶向性與細胞毒性藥物的高效性相結合的創新抗癌藥物。通過將高活性細胞毒素利用連接子與靶向腫瘤相關抗原的抗體偶聯,ADCs能夠實現對腫瘤細胞的精準打擊,同時減少對正常組織的毒副作用。
然而,ADCs存在固有局限性,其中一條便是藥物抗體比(Drug-to-Antibody Ratio, DAR)的限制。DAR是指每個抗體分子上偶聯的藥物分子數量,是影響ADCs療效和安全性的關鍵參數。為保證ADCs的結構穩定性、溶解度和藥代動力學性能,DAR一般不能超過8。因此,ADCs必須荷載毒性極強的藥物(IC50小于10 nmol),生產過程中未除盡的游離藥物以及脫靶效應將產生極大的毒性反應,限制ADCs的應用。
為克服ADCs的局限性,一類名為抗體-瓶刷前藥(Antibody– Bottlebrush Prodrug, BPD)偶聯物(Antibody– Bottlebrush Prodrug Conjugates, ABCs)的創新藥誕生。ABCs通過將單克隆抗體連接到BPDs構建而成。其中BPDs是納米級聚合物(長度和直徑約為10 nm),瓶刷的刷毛由親水性聚合物聚乙二醇(PEG)和與藥物相連的可剪切連接子組成。PEG外殼能有效隱藏負載藥物和連接子的化學特性,使各類ABCs保持統一的理化性質。通過調控BPDs合成過程,可精準調節DAR,使其比傳統ADC高出1-2個數量級,同時支持通過單一末端“點擊化學”手柄在抗體上實現隨機偶聯(賴氨酸)和位點特異性的偶聯(半胱氨酸)。(圖1)
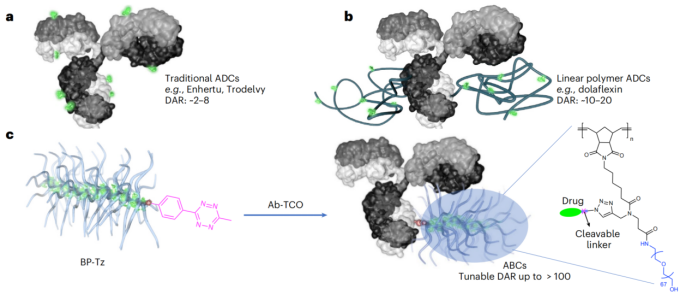
圖1. 傳統ADCs(a)、帶有線性聚合物鏈的ADCs(b)以及ABCs(c)的結構示意圖
通過開環復分解聚合(ROMP)合成BP和有效荷載的BP,隨后使用含有6-甲基-1,2,4,5-四嗪的炔烴終止劑終止反應,得到主鏈末端帶有單個四嗪的BP-Tz。BP-Tz的構建旨在通過反電子需求的Diels-Alder環加成反應與反式環辛烯(TCO)官能化的單克隆抗體偶聯。(圖2)
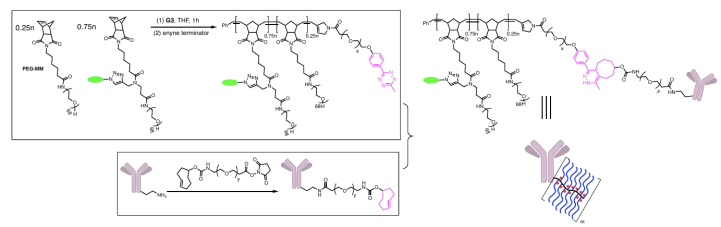
圖2. 在賴氨酸上隨機連接BP的ABCs合成方法
作者在靶向HER2的曲妥珠單抗(HER2-TCO)上連接六種不同荷載的BPD,BPD上分別帶有熒光基團(Cy5.5-Tz)、紫杉醇(PTX-Tz)、單甲基奧瑞他汀(MMAE-Tz)和SN-38(SN-38-Tz)(圖3d)。SDS-PAGE數據顯示,反應24小時內HER2-TCO即被完全消耗(圖3e)。
在ABCs體系中,DAR由BPD主鏈的聚合度以及單抗上BPD的平均數量共同決定(BPD-to-Antibody Ratio, BAR)。作者分別以BP-Tz:mAb-TCO=1:1至4:1的不同進料比例進行偶聯反應——當使用1:1投料時,主要結合產物的BAR為1;相比之下,當采用2:1比例時,mAb-TCO消耗殆盡,主要形成BAR為1或2的產物;進一步提高反應化學計量比可獲得更高的BAR。由于尺寸和電荷差異,可分離出BAR為1、2或3的結合物,從而研究BAR對抗原結合的影響(圖3f)。
作者通過微尺度熱泳(MST)和ELISA檢測法檢測ABC-HER2的結合親和力,結果表明ABC、單抗以及相應的ADC在與HER2的結合能力上并無顯著差異(圖3g)。流式細胞術檢測表明在表達HER2的細胞中,Cy5.5-HER2的攝取量顯著高于Cy5.5-IgG1和Cy5.5-BP(圖3h)。對于HER2+型細胞系,MMAE-HER2的IC50值相較于MMAE-BP大幅下降(圖3i),而對于HER2-型細胞系,兩者的作用效果基本一致。
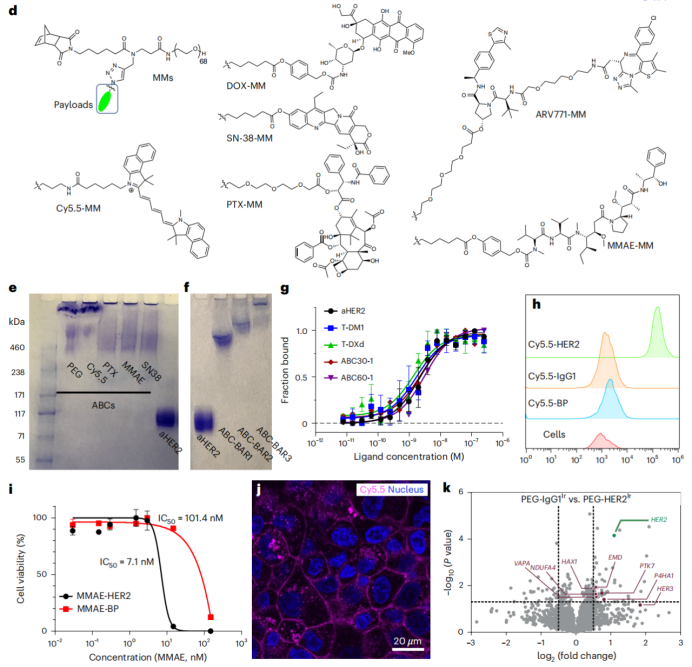
圖3. ABCs的構建和體外評價
需要指出的是,雖然上述方法可調控BAR,但無法精確控制結合位點——賴氨酸酯化是一個隨機過程。為驗證ABC合成與位點特異性單抗結合技術的兼容性,作者使用經過工程改造的曲妥珠單抗(含有兩個反應性半胱氨酸殘基)進行類似反應,成功制備出BAR值為1或2的位點特異性修飾ABC。(圖4)
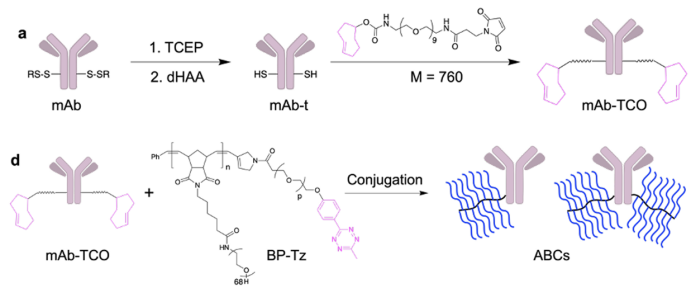
圖4. 在半胱氨酸上特異性修飾BP的ABCs合成方法
后續,作者通過大量動物實驗驗證ABCs具有長循環半衰期和高腫瘤積蓄;不同荷載的ABCs具有均有較好的療效,與相應臨床藥物相當甚至更優。除此之外,ABCs的荷載不局限于小分子藥物,作者測試荷載新型PROTAC藥物ARV771的ABC,仍能達到較好的腫瘤清除效果;抗體的選擇亦具有普適性,MMAE-MUC1對于MUC1+ CAOV-3卵巢癌細胞的IC50值遠低于MMAE-BPD的相應值。
總的來說,本文開發的ABCs通過“抗體 - 瓶刷前藥”的創新結構,突破了傳統ADCs的DAR限制、載荷范圍限制和設計靈活性限制,在體外和體內均展現出更高的靶向性、更強的療效和更低的毒性,且可適配PROTAC等新型載荷及多種腫瘤靶點。該技術為靶向癌癥治療提供了全新范式,具有明確的臨床轉化潛力,有望解決現有ADC難以覆蓋的低毒性載荷、低抗原表達腫瘤治療等臨床需求。
作者:WZH 審校:ZHR
DOI: 10.1038/s41587-025-02772-z
Link: https://doi.org/10.1038/s41587-025-02772-z








