苯胺類化合物作為關鍵結構單元,普遍存在于藥物分子及其他活性物質中,同時是多種工業材料制備的核心中間體。根據Transparency Market Research發布的《2021–2031年全球苯胺衍生物市場預測報告》顯示,至2031年全球苯胺類衍生物的市場價值將達到110億美元。因此,開發芳胺骨架的高效合成方法在藥物開發和材料科學等領域至關重要。傳統的苯胺類化合物的工業合成工藝主要以苯或其衍生物出發,通過苯環硝基化反應以及隨后的硝基苯催化加氫獲得苯胺。在醫藥中間體合成領域,過渡金屬催化的C–N鍵偶聯反應同樣被廣泛應用,這類方法的發展對于藥物分子的構建具有關鍵意義。盡管這些經典方法目前仍無可替代,科研工作者持續致力于探索更加綠色溫和、可持續的合成體系,從而最終避免使用高溫高壓的反應條件,或者高成本且具有生理毒性的過渡金屬催化劑。本研究聚焦生物酶催化體系的開發,通過定向進化初步驗證了該策略合成苯胺類化合物的可行性。值得注意的是,相較于自然界中存在的基于P450體系的苯胺合成酶,這一生物催化體系展現出截然不同的催化機制,為酶催化在苯胺合成領域的應用提供了新的突破方向。
近日,北京生命科學研究所 / 清華大學生物醫學交叉研究院劉臻課題組通過改造該實驗室開發的黃素(FMN)依賴酶PtOYE(源自Parageobacillus thermantarcticus),這一催化體系可以有效地將胺類化合物和環己酮衍生物組合,通過氧化胺化的機制制備多種二級和三級苯胺。針對結構不同的胺類底物,作者分別通過兩條定向進化路徑獲得了各自的優勢突變體OYE_G3和OYE_M3,提高了酶催化的效率并抑制了環己酮直接脫氫生成苯酚的副反應。通過多組動力學實驗,作者系統研究了這類苯胺合成酶的催化機制。實驗表明,優勢突變體不僅提高了亞胺中間體芳構化的催化效率,且降低了環己酮直接脫氫生成苯酚的活性,形成了有利于目標反應的協同效應。
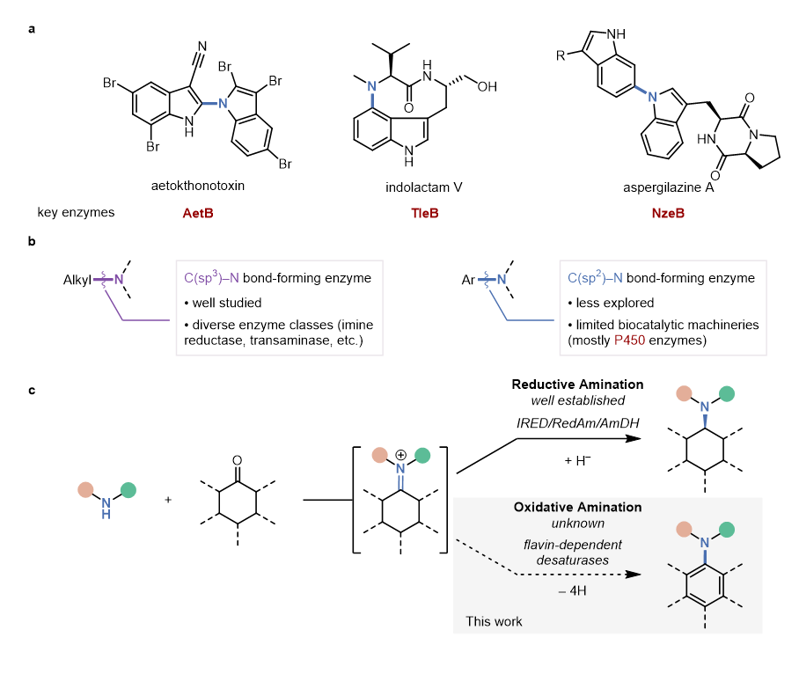
苯胺合成酶 (Aniline Synthase) 的開發過程
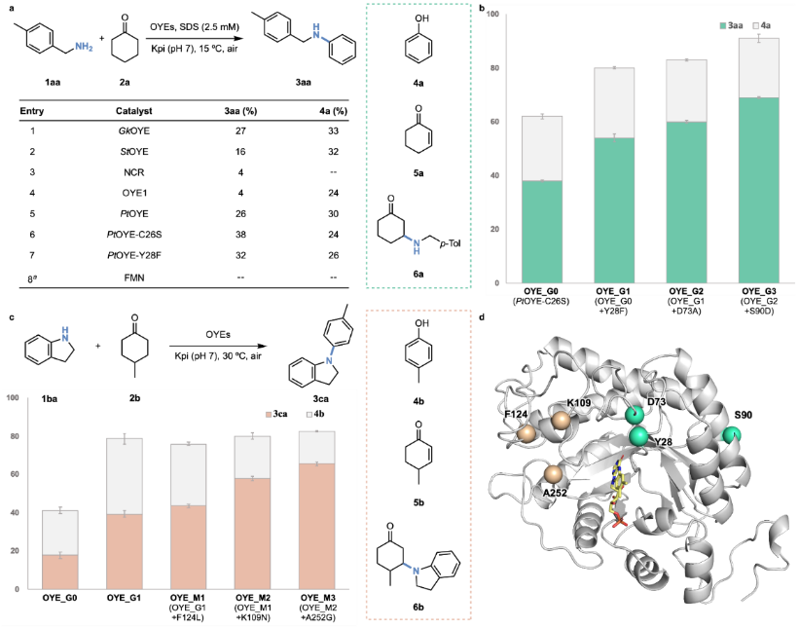
研究初期,作者首先對野生型黃素酶及其突變體的亞胺脫氫芳構化活性進行了系統性篩選。實驗數據顯示,課題組現有酶庫中的OYE_G0突變體對于目標反應具有顯著的初始活性,能夠以最高的轉化率(38%)催化生成目標產物3aa且目標產物與副產物4a的比例最優,體現了這類脫氫酶具有被進一步優化的潛力。
基于這一發現,研究人員隨后利用OYE_G0作為起始模版,分別針對二級苯胺和三級苯胺的合成過程進行了多輪蛋白質工程化改造與篩選。通過多個活性位點的定點飽和突變以及隨機突變,作者最終分別獲得催化合成二級苯胺的突變體OYE_G3以及催化合成三級苯胺的優勢突變體OYE_M3。
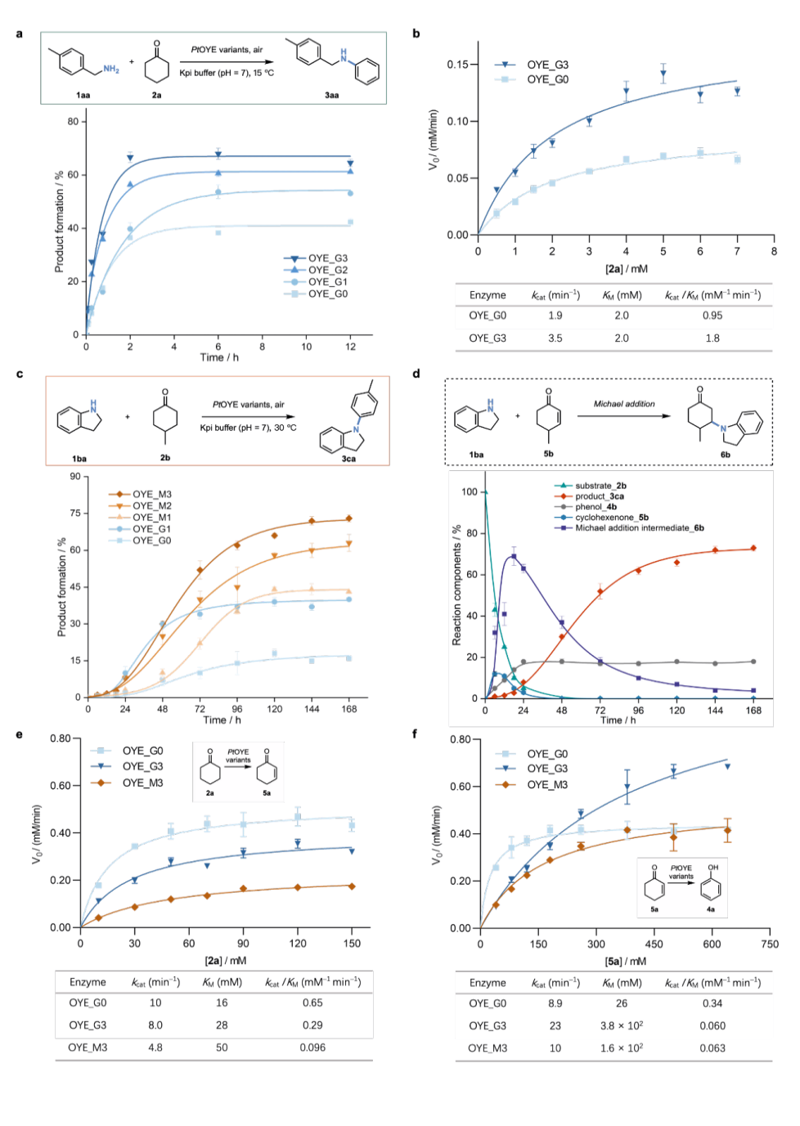
酶催化苯胺合成反應的底物探索與合成應用
在確定了最優酶突變體和最適反應條件之后,研究人員系統地研究了這些苯胺合成酶的底物適用范圍。結果表明,這種生物催化方法展示出了良好的底物兼容性和官能團耐受性,可以將不同取代的芐胺、含雜環的伯胺以及部分烷基胺轉化為相應的二級苯胺;也可成功地將部分仲胺轉化為三級苯胺。此外,不同取代模式的環己酮也能參與反應。在此基礎上,作者選取多個底物進行了制備規模的酶促反應,成功合成出如3ad、3ao等多種苯胺衍生物,進一步驗證了該方法的應用潛力。

酶促反應的機制研究過程
為了深入了解這一酶促反應的機理,作者對生物催化脫氫偶聯反應進行了一系列動力學研究。首先,研究人員使用二級苯胺合成酶進化譜系中的各個變體針對3aa的酶催化合成進行了時間進程實驗,并通過Michaelis-Menten曲線分析酶的動力學參數。實驗結果表明定向進化引入的突變有效地提高了苯胺合成酶OYE_G3的kcat。隨后,作者用類似的方法對三級苯胺3ca的合成反應進行了時間進程研究。與二級苯胺合成體系不同是,三級苯胺合成反應的前期會發生可逆的aza-Michael加成過程形成中間體6b,因此反應會顯示出明顯的誘導期(induction period)。為了明確探究酶活性是否從環己酮脫氫轉移到亞胺脫氫,作者比較了最初變體(OYE_G0)與定向進化譜系的兩個最終變體(OYE_G3和OYE_M3)生成苯酚的活性變化(圖4e和4f)。實驗結果表明,進化后的變體對于苯酚生成過程的催化能力顯著下降。
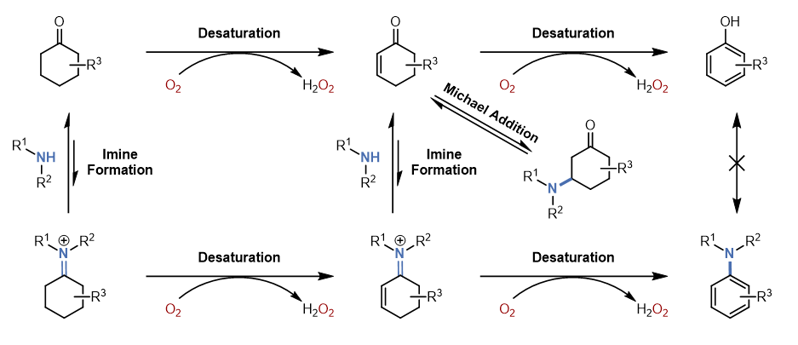
基于黃素依賴酶的獨特脫氫催化機制,作者開發了非天然的苯胺合成酶系統,可以有效地制備二級與三級苯胺衍生物。這種酶催化系統可以通過后續的進化進一步提高催化效率,并通過計算與實驗結合的方式完善機制研究。總體而言,這項工作為苯胺化合物的合成提供了高效、環境友好的生物合成策略,在生物催化和藥物開發等領域具有重要的應用前景。
論文信息
An Enzymatic Platform for Aniline Synthesis Through Oxidative Amination
Xiang Zhao, Zhen Liu
本項目的實驗部分主要由劉臻實驗室北師大學籍研究生趙翔完成。本研究得到科技部、清華大學生物醫學交叉研究院以及北京生命科學研究所的資助。
Angewandte Chemie International Edition
DOI: 10.1002/anie.202505252








